Publié le 23 mai 2018Lecture 8 min
Conduite à tenir devant une dermatite atopique sévère de l’adulte
Julien SENESCHAL, Service de Dermatologie de l'adulte et de l’enfant, Centre de référence pour les maladies rares de la peau (CRMRP), hôpital Saint-André, CHU de Bordeaux INSERM 1035, Immuno-Dermatologie ATIP-AVENIR Université de Bordeaux
Malgré la prise en charge locale par émollient et anti-inflammatoire et l’éducation thérapeutique, certaines formes sévères de dermatite atopique nécessitent le recours à un traitement systémique.
La dermatite atopique (DA) ou eczéma atopique est une dermatose inflammatoire chronique évo luant par poussées, associée à un prurit majeur touchant environ 10 à 20 % des enfants et 3 à 4 % des adultes. La prise en charge thérapeutique est parfois difficile car il est nécessaire à la fois de traiter les poussées aiguës de la maladie et de trouver la meilleure stratégie pour stabiliser la maladie sur le long terme. Également compte tenu du caractère chronique de la maladie, il est important d’éviter les potentiels effets secondaires des traitements locaux et généraux(1). L’échec de la prise en charge thérapeutique par soins locaux et/ou par photothérapie bien conduits reste rare. Cependant, certains adolescents ou adultes et plus rarement des enfants nécessitent une prise en charge par thérapie systémique quand les traitements locaux et/ou photothérapies et l’éducation thérapeutique restent insuffisants pour contrôler la maladie et assurer une qualité de vie correcte. Par ailleurs, les traitements systémiques peuvent être importants pour réduire la quantité de traitements anti-inflammatoires locaux chez les patients nécessitant quotidiennement de grandes quantités de soins locaux ou l’application sur de grandes surfaces cutanées. La prise en charge de la DA par thérapies systémiques concerne environ 10 % des patients. Les traitements systémiques les plus utilisés et efficaces, à l’heure actuelle, sont la ciclosporine A (CsA), seule à avoir l’AMM, le méthotrexate (MTX), l’azathioprine (AZA) et le mycophénolate mofétil (MMF), peu utilisé en France dans cette indication. L’utilisation d’une corticothérapie systémique, même si elle est efficace, doit être évitée du fait de son rapport bénéfice/risque non favorable.
L’utilisation des traitements systémiques immunosuppresseurs dans la DA n’est pas clairement codifiée. Il existe peu d’essais contrôlés randomisés les comparant, ce qui rend difficile l’évaluation de leur efficacité relative. La posologie de chaque traitement est à adapter au cas par cas en fonction de la sévérité de l’atteinte, des comorbidités de chaque patient, et par la suite en fonction de leur efficacité et de leur tolérance. La dose minimale efficace doit être utilisée afin de limiter la survenue d’effets indésirables (EI). Lorsque la DA est contrôlée et que le résultat se maintient, le traitement, en discussion avec le patient, peut être suspendu, avec parfois la possibilité de reprendre des soins locaux et/ou la photothérapie.
Ciclosporine (CsA)
La CsA est un immunosuppresseur appartenant à la famille des inhibiteurs de la calcineurine. Elle inhibe la production de cytokines inflammatoires comme l’interleukine (IL)-2, IL-3, IL-4 et le TNFα, et diminue la réponse immunitaire adaptative. Sa posologie varie de 3 à 5 mg/kg/j, à répartir en 2 prises par jour. L’efficacité de la CsA est constatée en général dans les 2 à 6 premières semaines de traitement. Plusieurs études ont évalué l’efficacité de la CsA dans la DA de l’adulte. Une revue systématique avec métaanalyse des essais contrôlés et non contrôlés concernant l’utilisation de la CsA dans la DA a été publiée en 2007(2). La sévérité de la DA sous CsA était retrouvée diminuée dans les 15 études (602 patients) analysées. Après 2 semaines de traitement, était notée une diminution moyenne de la sévérité de la DA de 22 % avec une dose de CsA de 2,5-3 mg/kg/j et de 40 % avec une dose de 4-5 mg/kg/j. Cependant, à 6 à 8 semaines de traitement, il n’y avait pas de différence d’efficacité entre ces 2 groupes de dose. Plus récemment, en 2010, est parue une étude rétrospective coréenne portant sur 147 patients ayant reçu de la CsA entre 2001 et 2008(3). La durée moyenne de traitement était de 13,5 mois et la dose moyenne initiale était de 2,7 mg/kg/j. Le SCORAD objectif était diminué en moyenne de 66,6 % à 6 mois de traitement, avec une amélioration déjà notée à 1 mois de traitement. La durée moyenne de rémission après arrêt de la CsA était de 4,5 mois. L’utilisation de la ciclosporine est limitée par ses effets indésirables et les nombreuses interactions médicamenteuses limitant son utilisation chez les sujets plus âgés prenant de nombreux traitements au long cours. Les effets indésirables (EI) sont principalement représentés par l’augmentation de la tension artérielle et du taux de créatininémie. Ces EI limitent souvent la durée du traitement par CsA au long cours à 1, voire 2 ans. Cependant, plusieurs études ont évalué sur des séries de patients l’utilisation en traitement continu de la CsA sur une période de 1 an. La tolérance était considérée comme bonne à très bonne chez 65 à 80 % des patients. Une augmentation significative de la créatininémie (> 30 % de la valeur initiale) était retrouvée chez 5 à 10 % des patients avec retour à la normale à l’arrêt du traitement. Les autres effets indésirables de la CsA sont des symptômes neurologiques (céphalées, paresthésies), souvent réversibles à l’arrêt du traitement, l’hypertrichose.
En dépit de son action immunosuppressive, la CsA, aux doses prescrites dans la DA, augmente peu le risque d’infections et si celles-ci surviennent, elles sont rarement sévères. Par ailleurs, il n’existe pas de majoration du risque d’infection opportuniste ou de réactivation tuberculeuse. Bien que quelques cas aient été décrits, il n’existe pas de preuve d’augmentation du risque de lymphome ou de cancer autre que cutané chez les patients traités par CsA dans une indication dermatologique.
Méthotrexate (MTX)
Le MTX est un antifolique inhibant la dihydrofolate réductase, empêchant ainsi l’activité de la thymidilate synthétase nécessaire à l’incorporation de nucléotides dans l’acide désoxyribonucléique (ADN). Le MTX peut être prescrit sous forme orale ou injectable, à une posologie variant en général de 7,5 mg à 25 mg une fois par semaine. L’efficacité du MTX, bien connue dans des pathologies inflammatoires chroniques, a aussi été mise en évidence dans la DA. Ainsi, Goujon et coll. ont évalué l’efficacité du MTX après 3 mois de traitement chez 20 patients et ont constaté une amélioration chez 75 % des patients (15/20)(4). Treize d’entre eux avaient une amélioration supérieure à 70 %. Un début d’amélioration était constaté entre le 1er et le 2e mois de traitement. En général, peu ou pas de gain d’efficacité est obtenu après un délai de 12 à 16 semaines de traitement, malgré une augmentation de la posologie. La même équipe a réalisé un essai randomisé chez l’adulte comparant le MTX à la CsA dans la DA modérée à sévère, présenté aux journées dermatologiques de Paris en 2014. Cette étude n’a pas montré de différence d’efficacité entre ces deux traitements, mais confirme l’intérêt du MTX dans cette indication. Cependant, la posologie du MTX dans cette étude n’était peut-être pas optimale et pourra être redéfinie dans de futures études.
Lyakhovitsky et coll. ont montré une amélioration chez 16 patients sur 20 après 2 à 3 mois de traitement à une dose de 10 à 25 mg/semaine, avec une amélioration moyenne du SCORAD de 44,3 % et du DLQI de 43,5 %. Le début de l’amélioration était constaté entre le 2e et le 3e mois de traitement. Le profil de tolérance semble similaire à celui des patients traités dans une autre indication, comme le psoriasis notamment. Les troubles digestifs tels que les nausées et les douleurs abdominales peuvent être améliorés en passant de la voie orale à la voie parentérale. La myélosuppression, responsable de leucopénie, thrombopénie et anémie, est souvent réversible après diminution ou arrêt du MTX. Des atteintes hépatiques (élévation transitoire des transaminases, voire fibrose hépatique lors de prises prolongées), pulmonaires (pneumo- pathies d’hypersensibilité en début de traitement, fibrose pulmonaire) et cutanéomuqueuses (érosions, ulcérations) peuvent également être constatées. Le risque infectieux aux doses prescrites pour la DA est faible et le risque de néoplasie est difficile à estimer.
Azathioprine (AZA)
L’AZA est un immunosuppresseur appartenant à la famille des inhibiteurs des bases puriques. L’AZA est prescrite à la dose de 1 à 3 mg/kg/j. La posologie doit être adaptée à l’activité de la thiopurine méthyltransférase (TPMT), enzyme intervenant dans le métabolisme de l’AZA, afin de limiter le risque de myélotoxicité. Pour cela, un génotypage du gène TPMT ou un dosage de l’activité enzymatique érythrocytaire de la TMPT peuvent être réalisés. Par ailleurs, une surveillance de la NFS et des enzymes hépatiques doit être réalisée régulièrement. L’efficacité de l’AZA a été démontrée dans des études rétrospectives, mais également dans des études contrôlées. Ainsi, un essai randomisé contrôlé ayant étudié l’AZA (1,5 à 2,5 mg/kg/j) versus MTX (10 à 22,5 mg/semaine) chez 42 adultes atteints de DA sévère a montré une réduction du SCORAD à 3 mois de traitement de 39 % dans le groupe AZA et de 42 % dans le groupe MTX, sans différence statistiquement significative en ce qui concerne l’efficacité des 2 traitements(5). L’efficacité de l’AZA peut être retardée, certains patients nécessitant 3 mois de traitement, voire plus, afin de constater une amélioration. Les troubles digestifs (nausées, vomissements, diarrhées, ballonnements, crampes, anorexie) sont fréquents sous AZA et peuvent être source de mauvaise observance. Ils peuvent être améliorés par une répartition de la dose ou une prise au cours d’un repas. La toxicité hématologique est proportionnelle à la dose et réversible à l’arrêt. Le risque carcinogène (et particulièrement de lymphome non hodgkinien et de carcinome épidermoïde cutané) est plus important chez es patients recevant des doses élevées et sur de longues périodes. Il est difficile d’estimer ce risque chez les patients traités par AZA dans l’indication de la DA.
Mycophénolate mofétil (MMF)
Cet immunosuppresseur bloquant la synthèse des purines s’est avéré efficace pour traiter la DA dans de petites études rétrospectives, à des doses allant de 0,5 à 3 g/j en 2 prises per os par jour. Cependant, le nombre d’études reste limité, ce qui ne permet pas d’apporter des conclusions précises sur son efficacité dans la DA. Par exemple, dans une étude portant sur 20 adultes, le MMF a permis une amélioration dès le 1er mois de traitement chez 17 patients, avec rémission complète permettant un arrêt du traitement chez 10 d’entre eux (les 7 autres étant contrôlés avec un traitement d’entretien). Les EI les plus fréquemment rapportés étaient des céphalées modérées, des symptômes digestifs et une asthénie. Plus récemment, une étude contrôlée randomisée a montré que le MMF était aussi efficace que la CsA dans le traitement d’entretien de la DA sévère de l’adulte, que son efficacité semblait toutefois moins rapide, mais qu’elle persiste plus longtemps après l’arrêt du traitement. Les EI étaient modérés et transitoires dans les 2 groupes.
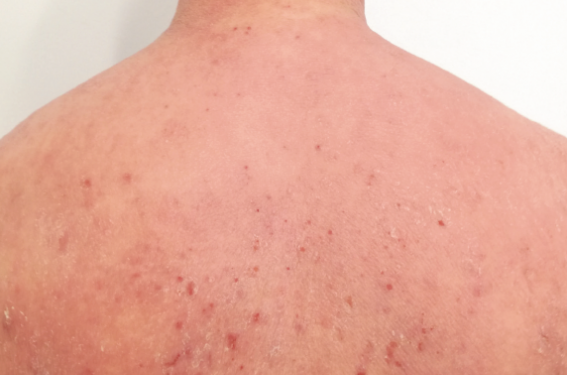
Peau sèche avec lichénification et lésions de grattage du dos chez un jeune adulte atopique.
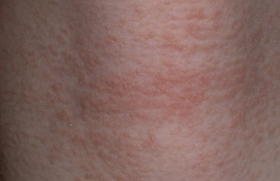
Lichénification des plis de flexion des genoux chez un adulte atopique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :