Publié le 31 oct 2022Lecture 4 min
Psoriasis de l’enfant - La place des biothérapies
Denise CARO, Boulogne-Billancourt
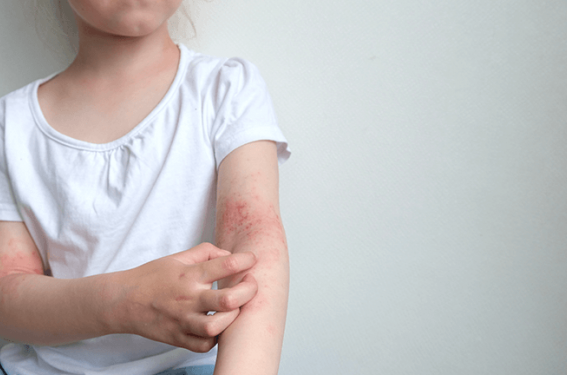
Selon les études 0,5 à 0,7 % des enfants âgés de 0 à 18 ans ont un psoriasis en Europe occidentale. En France, on estime que 100 000 enfants ont eu ou auront du psoriasis avant leur majorité ; et 10 à 20 % d’entre eux ont une forme sévère relevant d’un traitement systémique, par conséquent susceptibles de recevoir une biothérapie. Dans ce contexte, il importe de bien connaître le rapport bénéfice/risque de ces traitements chez l’enfant.
En 2021, cinq biothérapies étaient autorisées en Europe chez l’enfant atteint de psoriasis sévère.
Ce sont : deux anti-TNF-α, l’éta-nercept et l’adalimumab ; unanti-interleukine 12/23, l’ustékinumab ; et deux anti-IL-17, le sécukinumab et l’ixékizumab. Leur autorisation est fondée sur les essais cliniques, notamment les études de phase 3. Bien que nécessaires, ces essais ne reflètent pas totalement les prescriptions dans la vraie vie, d’où l’intérêt de compléter leurs enseignements par ceux émanant des études de cohorte.
Dans l’étude pivot évaluant l’efficacité et la tolérance de l’étanercept chez 106 enfants avec un psoriasis en plaques modéré à sévère, 57 % des patients avaient atteint un PASI 75 à S12(1). Une extension ouverte sur 5 ans a montré un bon profil de sécurité à long terme sans effets indésirables inattendus et le maintien de l’efficacité(2). L’étanercept a également été utilisé comme comparateur dans deux essais cliniques évaluant l’intérêt d’un anti-IL-17 dans le psoriasis en plaques sévère de l’enfant. Dans ces études, l’efficacité et la tolérance de l’étanercept étaient similaires aux données de l’étude pivot avec 63 % de PASI 75 et un bon profil de sécurité (3,4). Il convient toutefois de signaler que deux cas de tuberculose ont été rapportés dans l’étude pivot(1).
Autre anti-TNF-α, l’adalimumab a été évalué dans une étude de phase 3, conduite chez 38 enfants avec un psoriasis en plaques sévère; 57,9 % des patients ayant reçu une dose standard de 0,8 mg/kg avaient atteint un PASI 75 à 16 semaines. Une extension à 52 semaines, effectuée chez 108 enfants, a confirmé le maintien voire l’amélioration de l’efficacité à long terme(5). Par ailleurs, une revue systématique de la sécurité de ce médicament dans 7 essais cliniques impliquant des patients pédiatriques atteints de psoriasis, de rhumatisme ou de maladie de Crohn n’a pas identifié de nouvelle alerte concernant la tolérance de l’adalimumab(6).
L’ustékinumab (anti-IL-12/23) a fait l’objet d’un essai pivot portant sur 36 enfants de 12 à 17 ans atteints de psoriasis en plaques modéré à sévère
À 12 semaines, 80,6 % des adolescents avaient atteint un PASI 75. L’efficacité était maintenue à 52 semaines, et aucun nouveau signal de sécurité à long terme n'a été identifié(7).
Par ailleurs, un essai ouvert mené chez des enfants âgés de 6 à 12 ans prenant de l’ustékinumab a montré 84,1 % de PASI 75 à 12 semaines, avec une bonne tolérance(8).
Enfin, concernant les anti-IL-17A, l’ixékizumab a été évalué chez 115 enfants avec un psoriasis modéré a sévère et 39 enfants atteints de psoriasis en plaques sévère : après 12 semaines de traitement, respectivement 89 % et 84 % des patients avaient atteint un PASI 75(3). Et le sécukinumab, évalué chez 42 enfants avec un psoriasis en plaques modéré à sévère et 40 avec un psoriasis en plaques sévère, a permis d’obtenir respectivement 80,0 % et 92,9 % de PASI 75 à 12 semaines(4,9).
À noter qu’une « dose élevée », correspondant à la dose adaptée au poids normalement administrée à des patients adultes, n’a pas amélioré l’efficacité chez les enfants. Ce traitement à « dose élevée » (75/150/300 mg chez les enfants pesant < 25 kg, 25 à < 50 kg, ≥ 50 kg) pourrait toutefois être utilisé comme traitement de secours, après échec de la faible dose (75/75/150 mg chez les enfants pesant < 25 kg, 25 à < 50 kg, ≥ 50 kg) de 1re intention. Aucun effet indésirable spécifique à l’âge n’a été retrouvé avec les deux anti-IL-17A ; les effets les plus fréquents – rhinopharyngite et candidose – sont ceux rapportés chez les adultes. Il convient d’être prudent chez les enfants à risque de MICI(3,9).
> Les enseignements des cohortes
Des études rétrospectives récentes ont fourni des informations précieuses sur l’efficacité et la tolérance des biothérapies en pratique courante chez les enfants. Pour cela, on peut s’appuyer principalement sur 3 cohortes d’enfants atteints de psoriasis sous biothérapie :
la cohorte française BiPe à laquelle ont participé 30 centres a inclus 134 enfants de moins de 18 ans recevant 184 biothérapies ;
la cohorte rétrospective franco-italienne BiPe Jr qui a inclus 82 enfants de moins de 12 ans avec 106 biothérapies ;
la cohorte Chi-PsoCov d’enfants ayant contracté la Covid alors qu’ils étaient sous biothérapie pour un psoriasis.
La cohorte BiPe nous apprend que jusqu’à 72 % des enfants traités par biothérapie en pratique courante n’auraient pas été inclus dans les essais cliniques en raison de comorbidités, du type clinique de leur psoriasis (non en plaques), de traitements concomitants, de critères de gravité ou parce qu’ils étaient trop jeunes(10). Or, le profil de tolérance des biothérapies dans les cohortes est le même que dans les études cliniques ou celui constaté chez l’adulte (par exemple, concernant le risque d’infection ou de prise de poids chez les patients recevant un traitement anti-TNF-α)(11,12). Par ailleurs les cohortes permettent de comparer les différentes biothérapies en pratique courante. Ainsi, d’après les données de BiPe et BiPe Jr, l’adalimumab et l’ustékinumab ont un meilleur taux de maintien à 1 an que l’étanercept(13).
Les biothérapies ont révolutionné la prise en charge du psoriasis sévère de l’enfant. Si des réticences sont encore présentes, notamment du fait du coût et d’un développement récent, leur profil efficacité/tolérance est favorable. Le nombre de cas par année de traitement est plus faible avec les biothérapies qu’avec les traitements systémiques classiques proposés dans les formes sévères de psoriasis chez l’enfant(14).
D’après la communication d’Emmanuel Mahé (Argenteuil)
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :