Maladie de système, Médecine interne
Publié le 01 sep 2023Lecture 7 min
Hidradénite suppurée - Le point de vue du dermatologue
La maladie de Verneuil ou hidradénite suppurée est une maladie inflammatoire chronique du follicule pilo-sébacé fréquente (1 à 4 % de la population occidentale), associée à un impact majeur de la qualité de vie(1). Ses causes sont multiples, rassemblant des facteurs à la fois génétiques et liés à l’environnement ou au mode de vie (tabac, surpoids, facteurs hormonaux). Si sa physiopathologie est encore non totalement élucidée, sa meilleure compréhension permet de découvrir de nouvelles cibles thérapeutiques.
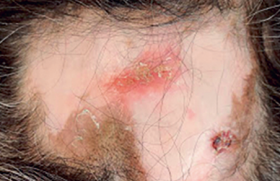
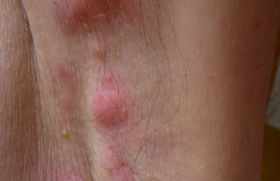
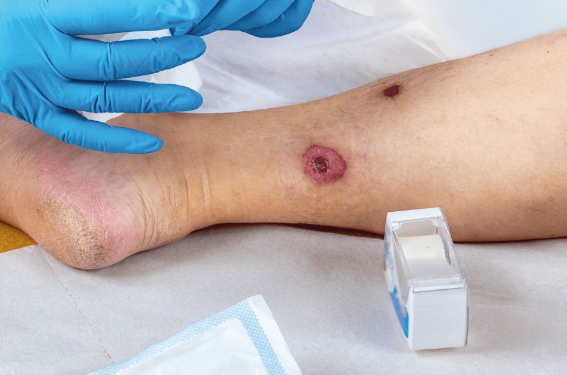
Le diagnostic d’hidradénite suppurée (HS) est clinique. Les lésions incluent des nodules, des abcès, des fistules ou des cicatrices hypertrophiques en corde dans les plis et les zones folliculaires (figure 1[2]). Le diagnostic repose sur 3 critères :
– des nodules et des abcès douloureux évoluant vers la suppuration, la fistulisation et/ou la formation de cicatrices ;
– des localisations typiques : aisselles, plis inguinaux, région périanale et/ou périnéale, seins et plis sous-mammaires, pli inter-fessier, pubis ;
– un caractère chronique et récidivant des lésions : au moins 2 poussées en 6 mois.
Figure 1. Lésions cutanées retrouvées dans l’hidradénite suppurée (adapté de Van Straalen et al. Journal of Allergy and Clin Immunol Avril 2022).
Il n’est pas indiqué de réaliser des prélèvements microbiologiques, sauf en cas de fièvre, car celle-ci est inhabituelle dans l’HS. Il existe une association statistique de la maladie de l’HS avec d’autres pathologies à rechercher :
– inflammatoires : spondylarthropathies, maladies inflammatoires de l’intestin (maladie de Crohn, rectocolite hémorragique), acné conglobata, syndrome métabolique ;
– génétiques : Dowling-Degos, pachyonychie congénitale ;
– tumorales : carcinome épidermoïde, lymphome ;
– psychiatriques (dépression, fréquente et à rechercher).
Certaines formes syndromiques peuvent être également associées à l’HS, et doivent être recherchées. Elles incluent l’association de plusieurs maladies auto-inflammatoires telles que l’acné, le pyoderma gangrenosum, l’arthrite pyogénique ou les spondylarthropathies :
– PASH : pyoderma gangrenosum, acné, hidradénite suppurée ;
– PASS : pyoderma gangrenosum, acné, hidradénite suppurée, spondylarthrite ankylosante ;
– PAPASH : arthrite pyogénique, pyoderma gangrenosum, acné, hidradénite suppurée ;
– PsAPASH : rhumatisme psoriasique, pyoderma gangrenosum, acné, hidradénite suppurée.
Par ailleurs, l’HS peut aussi être associée à des maladies auto-inflammatoires telles que la fièvre méditerranéenne familiale.
Enfin, l’HS fait partie de la tétrade d’occlusion folliculaire, comprenant en plus de l’HS l’acné conglobata, la cellulite disséquante du cuir chevelu, et le sinus pilonidal.
Il existe plusieurs scores de sévérité permettant d’évaluer la maladie ; ils sont rassemblés dans le tableau 1.
PHYSIOPATHOLOGIE(1,2)
La physiopathologie de l’HS n’est pas encore totalement élucidée. Certains facteurs associés ou facteurs de risque sont décrits.
• Facteurs génétiques : les cas familiaux sont fréquents et l’héritabilité de l’HS est décrite autour de 80 %. Des mutations ont été décrites dans les gènes codant pour les sous-unités du complexe de la gamma-sécrétase (PSEN1, PSENEN, APH1B, NCSTN), mais ces mutations représentent un faible pourcentage des cas familiaux, suggérant d’autres mutations non encore décrites.
• Facteurs exogènes : tabac, obésité.
L’événement initial (figure 2) est associé à une occlusion et une stase folliculaires (d’origine génétique, favorisée par la nicotine ou les frottements mécaniques liés aux plis), entraînant un infiltrat inflammatoire périfolliculaire. La libération de DAMPs (Danger-Associated Molecular Pattern) active les cellules immunitaires et la sécrétion de cytokines pro-inflammatoires (TNF, IL1bêta) conduisant à la sécrétion de chémokines (CXCL8, CXCL11, CCL20, CCL2…) et à l’infiltration périfolliculaire et périvasculaire par des cellules immunitaires (lymphocytes T [Th17 et Th1], lymphocytes B, monocytes) produisant notamment IL-17 et IFN-gamma.
Figure 2. Étapes initiales de la physiopathologie de l’hidradénite suppurée. Occlusion folliculaire à l’origine de l’inflammation du follicule pileux (adapté de Sabat et coll.(1)).
La progression vers les stades plus avancés et l’inflammation chronique se manifeste par la dilatation du follicule pileux conduisant à sa rupture et au relargage de son contenu, ce qui amplifie la réponse inflammatoire et se traduit cliniquement par un nodule inflammé ou un abcès, la formation de pus, et la destruction tissulaire. La compréhension de ces différentes étapes permet d’identifier de nouvelles cibles thérapeutiques afin d’élargir l’arsenal de traitement.
PRISE EN CHARGE THÉRAPEUTIQUE*
Mesures générales
Il est recommandé de promouvoir le sevrage tabagique et la perte de poids(3). Si le surpoids et l’obésité sont des facteurs de risque et de résistance thérapeutique de plusieurs maladies inflammatoire (notamment dans le psoriasis[4]), la perte de poids dans l’HS permet également de diminuer le frottement de peau à peau dans les plis.
Par ailleurs, une éventuelle prise en charge psychologique et de la douleur est indiquée quand nécessaire.
Antibiothérapie
Aucune étude sur l’efficacité des antibiotiques est de fort niveau de preuve. Il n’y actuellement pas d’efficacité curative démontrée d’une antibiothérapie à large spectre au long cours ou répétée. Trois indications d’antibiothérapie sont retenues dans l’HS : poussée aiguë d’HS Hurley I/II ; traitement d’attaque avant chirurgie de la zone atteinte ; prophylaxie secondaire.
• Poussée aiguë d’HS Hurley I/II
Augmentin 50 mg/kg ou pristinamycine 3 g/jour pendant une semaine.
• Hurley II/III
La prise en charge est médicochirurgicale. Traitement d’attaque avant chirurgie de la zone atteinte par ceftriaxone 1 à 2 g/j IM + métronidazole PO 3 x 500 mg/jour OU lévofloxacine (500 mg, 1 à 2 fois/jour) + clindamycine (600 mg, 3 fois/jour), sur une durée maximale de 15 à 21 jours ; suivi d’une chirurgie de la zone atteinte ; suivi d’une prophylaxie secondaire (doxycycline 100 mg/jour, OU cotrimoxazole 400/80 mg/jour) OU traitement biologique.
• Prophylaxie secondaire
Quel que soit le grade, dont l’efficacité doit être réévaluée entre 3 et 6 mois : prévention des récurrences si au moins 4 poussées par an ; doxycycline 100 à 200 mg/jour ou cotrimoxazole 400/80 mg/jour.
Biologiques
• Les anti-TNF
Les anti-TNF sont recommandés d’emblée en cas de maladie sévère avec une altération importante de la qualité de vie (DLQI > 11) ou en cas d’échec des antibiotiques. Le traitement recommandé des for mes associées à des maladies inflammatoires, telles que maladies inflammatoires de l’intestin ou la spondylarthropathies, est un traitement à partir d’anti-TNF (adalimumab ou infliximab) dont l’efficacité doit être réévaluée à 6 mois.
L’adalimumab - Les essais de phase III PIONEER I et II rapportent une amélioration du nombre de lésions à semaine 12 de traitement chez 50 % des patients, contre placebo. Cette bonne réponse était maintenue à 3 ans chez 50 % des patients(5,6).
Depuis mars 2021, la Haute Autorité de santé a émis un avis favorable pour son remboursement dans l’HS active modérée à sévère de l’adulte en cas de réponse insuffisante au traitement systémique conventionnel de l’HS.
Son schéma de prescription est le suivant :
– Traitement d’attaque S0 : 160 mg SC S2 : 80 mg SC
– Traitement d’entretien : 40 mg par semaine OU 80 mg toutes les deux semaines. Les données des essais cliniques suggèrent d’atteindre une concentration sérique > 7-8 μg/mL à S2 et 7-11 de S12 à S36(5,6).
L’infliximab - L’infliximab n’a pas d’AMM dans l’HS. Les recommandations de la Société française de dermatologie proposent cependant son utilisation uniquement par des équipes expertes dans la prise en charge de patients atteints d’HS sévères ou résistantes aux premières lignes de traitement. Aucune donnée prospective n’est à ce jour disponible concernant le monitoring de son dosage sérique ou de la présence d’anticorps neutralisant, cependant une étude rétrospective monocentrique rapporte qu’une concentration sérique < 7 μg/mL serait associée à une absence de réponse clinique(7).
Une étude rétrospective monocentrique rapporte l’efficacité du sirolimus en adjonction à un traitement anti-TNF (infliximab ou adalimumab) chez des patients présentant une HS sévère et réfractaire à de hautes doses s d’anti-TNF(8). Il s’agit d’une utilisation, hors recommandations, et par un centre expert pour ces cas particulièrement sévères.
• Essais en cours des petites molécules et autres biologiques
De nombreux essais thérapeutiques engageant des biothérapies ciblant notamment des cytokines pro-inflammatoires sont en cours. Aucun n’est recommandé à ce jour : anti- IL1 (NCT01558375), anti-IL23 (NCT03628924, NCT03926169), inhibition du récepteur au CXCR1 et CXCR2 (NCT04493502), inhibition de l’IL-36R (NCT04856930). Des petites molécules sont également en cours d’essai, notamment : inhibiteurs de Janus kinase 1 (NCT03569371 et NCT03607487), inhibiteurs d’IRAK4 (NCT04772885).
CONCLUSION ET PERSPECTIVES
L’hidradénite suppurée est une maladie inflammatoire chronique fréquente du follicule pileux.
L’occlusion folliculaire est à l’origine d’un infiltrat inflammatoire conduisant à une inflammation chronique et une destruction folliculaire.
Le traitement dépend du stade, de la sévérité et du retentissement. Les indications de l’antibiothérapie sont bien définies ; celle-ci ne doit pas faire appel à une antibiothérapie à large spectre prolongée ou répétée. Les formes sévères ou résistantes sont prises en charges par anti-TNF, de nombreux essais sont en cours concernant d’autres biologiques ou thérapies ciblées mais ne font pas l’objet de recommandations actuellement.
Une meilleure compréhension de la physiopathologie permet d’élargir l’arsenal de traitements par la découverte de nouvelles cibles thérapeutiques.
POINTS FORTS
• L’HS est une maladie inflammatoire chronique du follicule pileux fréquente.
• Le diagnostic est clinique, et doit comprendre la recherche de comorbidités, facteurs favorisants, sévérité et impact sur la qualité de vie.
• La physiopathologie comprend 2 étapes : l’occlusion folliculaire, entraînant un infiltrat inflammatoire du follicule pileux, et la chronicisation de l’inflammation à l’origine de la destruction du follicule pileux.
• Le traitement dépend de la sévérité, des comorbidités associées et de l’impact sur la qualité de vie.
• L’antibiothérapie a trois indications (traitement d’attaque, préopératoire, prophylaxie secondaire).
• Les anti-TNF sont indiqués dans les formes sévères et résistantes.
• De nombreux essais sont en cours pour élargir l’arsenal thérapeutique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :