Publié le 10 mar 2025Lecture 6 min
Prise en charge actuelle de la folliculite décalvante
Catherine FABER, d’après la communication de Bruno Matard

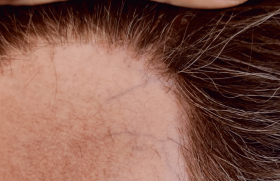
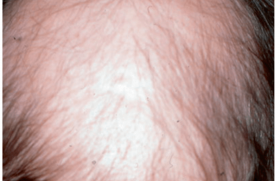
La folliculite décalvante est une maladie très polymorphe avec de nombreux pièges diagnostiques. À ce jour, aucun traitement ne permet sa guérison complète, mais des rémissions prolongées peuvent être obtenues.
La folliculite décalvante (FD) pose des problèmes de diagnostic différentiel avec le lichen à l’origine d’une controverse nosologique, de physiopathologie, qui est mal comprise, et de traitement. Cette maladie d’évolution cicatricielle potentiellement sévère se caractérise par une atteinte qua si exclusive du cuir chevelu, une survenue à l’âge adulte – jamais avant la puberté –, une prédominance masculine et l’absence d’antécédent familial ou de maladie associée dans l’immense majorité des cas. La lésion élémentaire est une folliculite destructrice à polynucléaires neutrophiles (PNN), avec une implication de la voie Th17. Elle débute au niveau des follicules pileux (FP) et s’arrête avec leur destruction. Le FP apparaît donc à la fois comme le lieu de la cause de l’inflammation et de la chronicité. La chronicité indéfinie de la FD est plus ou moins longue, mais toujours transitoire avec les antibiotiques ciblant Staphylococcus aureus, qui est trouvé dans la peau atteinte dans la majorité des cas(1). Les prélèvements de peau lésionnelle montrent aussi la présence d’autres bactéries de la flore transitoire, dont de nombreux bacilles Gram négatifs. Les caractéristiques de S. aureus, notamment l’absence de toxicité spécifique et sa sensibilité habituelle à la plupart des antibiotiques, suggèrent qu’il agit comme un agent opportuniste plutôt que pathogène. Il a été montré que le microbiote sous-épidermique est lui aussi dominé par de la flore transitoire. Ce constat plaide pour une anomalie de la barrière épidermique de cause inconnue.
Une pathologie récidivante
Après traitement antibiotique, l’inflammation diminue mais ne dis paraît jamais complètement. On note la persistance d’un microbiote sous-épidermique anormal qui pourrait agir comme un réservoir et serait la cause des récidives(1). Il persiste également un érythème et une hyperkératose péripilaires, donnant un tableau clinique de lésion pseudolichénienne. Une classification élaborée pour évaluer l’efficacité des anti-TNF dans la FD permet de quantifier l’inflammation (score FD-IGA)(2). Elle comporte cinq stades de 0 (inflammation absente) à 4 (inflammation sévère). Le stade 2 (inflammation légère) est défini par la présence d’un érythème et/ou d’une hyperkératose strictement périfolliculaires, sans pustule ni croûte. Il correspond à la forme « lichen-like » dont la description a conduit à l’hypothèse d’un spectre phénotypique FD/lichen plan pilaire (LPP)(3,4). Mais celle-ci est réfutée par des travaux ayant montré que ces deux maladies ont des profils immunitaires différents(5). L’évolution naturelle de la FD suffit à expliquer ces aspects cliniques(6). De fait, l’infiltrat à PNN qui la caractérise est fugace en raison de la courte durée de vie de ces cellules dans les tissus. Cet infiltrat neutrophilique situé à la superficie du FP évolue rapidement vers un infiltrat lympho-plasmocytaire à sa partie profonde. On observe une destruction de l’unité folliculaire et la formation d’un granulome périfolliculaire.
Des diagnostics différentiels
Dans le cadre de la FD, le problème diagnostique le plus fréquent est le LPP. Il se pose devant de formes stables et non évolutives. Au stade tardif, la notion de pustules et de croûtes dans l’évolution ainsi que la présence d’un saignement et d’une polytrichie sont en faveur de la FD. En cas de doute clinique, la biopsie permet de trancher en mettant en évidence un infiltrat lympho-plasmocytaire sans dermatite d’interface dans la FD ou un infiltrat lichénien avec une dermatite d’interface plus ou moins dense dans le LPP. L’épaississement de l’épithélium interfolliculaire est un argument histologique supplémentaire en faveur de la FD(7,8).
D’autres diagnostics différentiels doivent être évoqués tels que le psoriasis devant une forme hyperkératosique de FD, le lupus dans certaines formes inflammatoires et la cellulite disséquante du scalp dans les formes papuleuses et/ou chéloïdiennes.
Enfin, devant une suspicion de FD, il faut systématiquement réaliser un prélèvement mycologique afin d’exclure le diagnostic de teigne.
Une prise en charge difficile
Le traitement de la FD n’est pas codifié. Aucun des traitements proposés n’a fait l’objet d’étude contrôlée. La plupart des données thérapeutiques publiées sont issues d’études de faible niveau de preuve et les traitements actuels ne sont pas curatifs. Le rationnel du traitement est de diminuer la charge bactérienne des bactéries putatives et l’inflammation. Une autre option possible est la destruction du FP par laser Nd-YAG. À noter que la radiothérapie est à proscrire dans cette indication. L’efficacité thérapeutique est évaluée sur les signes cliniques et fonc tionnels (douleur, prurit, saignement), en utilisant la classification de l’inflammation et des photos avec le smartphone du patient afin d’avoir un suivi objectif. Le rythme de suivi sera plus ou moins fréquent selon l’évolutivité.
Les tétracyclines sont le traitement antibiotique général le plus fréquemment utilisé dans la littérature et dans la pratique. Il existe un consensus relatif sur leur prescription en première intention pendant plusieurs mois jusqu’à l’obtention d’un stade 2 IGA-FD. L’antibiothérapie de deuxième intention repose sur l’association rifampicine et clindamycine pendant 10 semaines. L’amoxicilline-acide clavulanique pendant 1 à 2 semaines (en première ligne) ou le sulfaméthoxazole-triméthoprime pendant plusieurs mois (en deuxième ligne) sont volontiers prescrits en alternative. D’autres antibiotiques généraux peuvent être utilisés, mais plutôt en deuxième ligne dans des situations de contre-indications ou dans des circonstances particulières. Une antibiothérapie locale par érythromycine solution (Eryfluid®), clindamycine (Zindacline®), acide fusidique topique 2 % (Fucidine®), sulfadiazine argentique crème (Flammazine®) ou mupirocine 2 % pommade peut être associée.
L’arsenal thérapeutique anti-inflammatoire comprend des traitements locaux (dermocorticoïdes [DC] de classe très forte ou forte, corticoïdes intralésionnels en cas de lésions fibrosantes ou lichénifiées, tacrolimus topique 0,1 %) et des traitements généraux incluant la dapsone, le zinc ainsi que les biothérapies et immunomodulateurs. Ces deux dernières classes thérapeutiques sont peu ou mal évaluées dans la FD, les données disponibles émanant uniquement de cas isolés et de petites séries. Parmi les publications, l’étude ayant la meilleure méthodologie, avec une efficacité évaluée à l’aide du FD-IGA, a mis en évidence une bonne réponse chez 5 patients sur 11 après 6 mois de traitement par anti-TNFα(2). Ces résultats nécessitent une confirmation.
Par ailleurs, la photothérapie dynamique (PDT) est en théorie intéressante(10-12) et l’utilisation d’un dispositif textile lumineux permet une réduction significative de la douleur et une meilleure répartition de l’énergie lumineuse(13). Mais là encore, la littérature actuelle ne comporte que quelques séries et cas isolés (n = 32 patients) et quelques échecs ont été rapportés(14). La PDT doit être mieux évaluée dans la FD. En ce qui concerne l’isotrétinoïne, son efficacité est évoquée dans deux études plus que discutables et qui n’auraient jamais dû être publiées(15,16). L’expérience de la majorité des auteurs montre que, contrairement à leurs résultats, ce traitement n’est pas efficace dans la FD.
Quant aux greffes folliculaires, elles étaient plutôt déconseillées jusqu’alors en raison du risque théorique de récidive et au vu de quelques cas rapportés en 2009 de FD survenue après des greffes pour alopécie androgénique(17). Il n’y a pas de publications sérieuses écentes sur le sujet. Des résultats assez satisfaisants ont été rapportés par deux patientes (expérience personnelle) qui ont eu des récidives tardives, à 3,5 ans et 4,5 ans, relativement contrôlées par le traitement. En attendant de mieux préciser leur place dans la prise en charge de la FD, les greffes folliculaires ne doivent être proposées qu’à des patients qui acceptent le risque de récidive, même très longtemps après. Elles devront être faites après au moins 1 an au stade 0 ou 1 et des greffons test laissés en place pendant la même durée. Un essai multicentrique français évaluant l’intérêt de trois molécules biologiques dans le traitement de la FD devrait débuter cette année. Cette étude dite « BOOSTERS » (BiOlogics in FOlliculitis decalvanS : adaptaTivE tRialS), financée par un PHRC, répond au besoin de recherche sur cette maladie.
D’après la communication de Bruno Matard, Centre Sabouraud, hôpital Saint-Louis, Paris.
Flash pour la pratique, JDP 2024.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :