Dermatologie générale
Publié le 04 jan 2020Lecture 10 min
Le lichen plan est une maladie inflammatoire des épithéliums malpighiens avec possibilité d’une atteinte cutanée, muqueuse, phanérienne. Parmi les muqueuses, l’atteinte buccale est la plus fréquente, l’atteinte génitale plus rare, les atteintes œsophagienne, conjonctivale ou des conduits auditifs externes sont exceptionnelles. L’atteinte phanérienne touche les ongles et le cuir chevelu.
La prévalence du lichen plan buccal (LPB) est de 0,5 à 3 % suivant les régions (2,2 % chez les femmes suédoises) avec un ratio femme/homme de 1,5 à 3/1. L’âge d’apparition est surtout entre 30 et 60 ans. Une atteinte génitale est associée dans 20 % des cas, une atteinte cutanée dans 15 %, alors qu’une localisation buccale est mise en évidence dans 70 à 77 % des lichen plans cutanés(1).
CLINIQUE
Le LPB a de nombreuses formes cliniques différentes ; il peut être blanc (réticulé le plus fréquemment ou en plaques ou verruqueux), pigmenté, érythémateux, érosif ou bulleux, atrophique. Le début est insidieux ou brutal. Il peut toucher toutes les régions de la cavité buccale. Les sites affectés sont par ordre décroissant la muqueuse jugale, la langue (faces dorsales et latérales), la gencive, le palais, la demi-muqueuse labiale et enfin le plancher buccal. La muqueuse jugale postéro-inférieure constitue la zone de prédilection avec une atteinte généralement bilatérale et symétrique.
Le lichen plan réticulé est typiquement asymptomatique, souvent de découverte fortuite. Il est formé de lésions punctiformes kératosiques de couleur blanche qui vont peu à peu confluer pour former réseau blanchâtre le plus souvent en feuille de fougère (figures 1 et 2).
D’autres assemblages sont possibles réalisant des lésions annulaires, circinées, en mottes (figure 3).
Ailleurs, il peut former des plaques blanches leucoplasiques plus ou moins verruqueuses (figures 4 et 5 voir page 10).
Le diagnostic différentiel des lésions blanches est aisé en cas de lésions réticulées ; il faut toutefois éliminer des lésions de lupus discoïdes similaires dans la bouche à un lichen plan, généralement associées à des lésions cutanées. Les formes en plaques leucoplasiques doivent faire éliminer une leucoplasie tabagique par le contexte, la localisation différente, unilatérale et asymétrique.
Chez les sujets à peau déjà pigmentée, le lichen plan est parfois pigmentogène du fait de l’incontinence pigmentaire induite par la nécrose des kératinocytes, laissant une pigmentation irrégulière réticulée (figure 6) à différencier d’une pigmentation ethnique.
L’apparition d’une rythème témoigne généralement d’une poussée d’activité de la maladie, occasionnant des douleurs spontanées ou lors de la prise de certains aliments, notamment épicés. L’erythème entoure les lésions blanches ou apparaît au centre des lésions (figure 7) facilitant le diagnostic ; il est plus rarement isolé.
Le lichen plan érosif se caractérise par des zones muqueuses érodées et douloureuses à limites nettes, recouvertes de pseudomembranes, sur un fond rouge, associé ou non à un réseau lichénien réticulé. Il siège préférentiellement sur la face interne des joues, la langue (figure 8) et les gencives (figure 9).
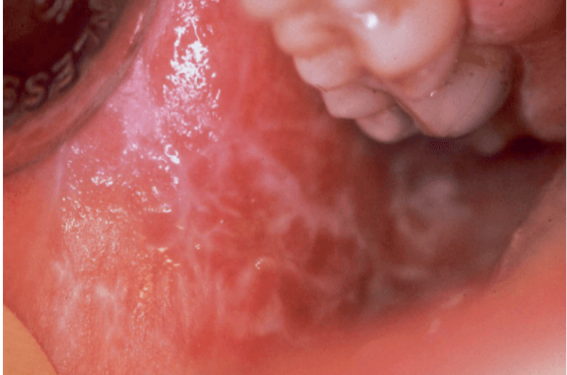
La localisation gingivale est significativement associée chez la femme à une localisation vulvo-vaginale (figure 10).
Elle doit être différenciée d’une pemphigoïde cicatricielle responsable comme le lichen plan d’une gingivite érosive. Un aspect d’érosions recouvertes de pseudomembranes est très évocateur de pemphigoïde cicatricielle lorsqu’il s’associe au signe de la pince. La traction de l’une de ces pseudo-membranes avec une pince fait apparaître une érosion post-bulleuse témoignant de la fragilité de la zone de jonction dermo-épidermique. L’atteinte oculaire est fréquente dans la pemphigoïde cicatricielle, alors qu’elle est rare dans le lichen plan.
Les formes atrophiques peuvent apparaître d’emblée ou plus souvent secondairement après plusieurs années d’évolution. Elles sont observées plus volontiers sur les gencives qui s’irritent lors du brossage des dents et le dos de la langue, provoquant une dépapillation, rendant la langue plus sensible aux aliments épicés.
DIAGNOSTIC
La multitude des formes cliniques de LPB contraste avec l’unicité des lésions histologiques. Il est préférable de réaliser la biopsie muqueuse sur une zone blanche, non érosive ou atrophique (stade séquellaire). L’aspect anatomopathologique est typique avec un infiltrat lymphocytaire en bande limité à la partie superficielle du chorion, associé à une nécrose des cellules formant l’assise épithéliale basale sans dysplasie épithéliale (figure 11).
La biopsie n’est pas nécessaire en présence d’une forme typique de LPB blanc réticulé ; elle est souhaitable dans les autres formes, notamment érosive ou leucoplasique et indispensable en cas de prescription d’un traitement agressif. L’immunofluorescence directe en peau atteinte, souvent positive de manière non spécifique (dépôts de fibrinogène au niveau de la membrane basale), n’est pas réalisée exceptée en cas de doute diagnostique avec une pemphigoïde cicatricielle ou un lichen plan pemphigoïde (association des 2 affections). La séparation entre LPB, lésions lichénoïdes buccales et lésions lichénoïdes buccales induites est souvent difficile cliniquement et histologiquement, d’où une attitude pratique commune dans toutes ces affections. Les lésions lichénoïdes diffèrent théoriquement du LPB par un aspect clinique et histologiques ressemblant plus ou moins fidèlement à un LPB ; celles induites disparaissent après élimination du facteur inducteur (contact, médicamenteux, systémique).
BILAN
Un examen de la peau et de toutes les muqueuses permettra de dépister des localisations extra-buccales de lichen. De nombreuses associations au LPB ont été décrites notamment avec l’hépatite C, le lien statistique entre LPB et hépatite C étant récusé dans de nombreux pays, plus fortement en Italie que dans les pays nordiques ; toutefois, étant donné les traitements efficaces de l’hépatite C, il paraît raisonnable de demander au moins une fois un bilan hépatique et une sérologie d’hépatite C. Les autres associations ne justifient pas de recherche systématique du fait d’un diagnostic évident comme au cours d’une réaction du greffon contre l’hôte, d’un lien faible, voire inexistant, tel qu’avec le diabète, ou la rareté de l’affection comme le thymome.
Une cause médicamenteuse doit être systématiquement recherchée. Pour beaucoup d’auteurs, il n’y a pas de différence clinique ou histologique entre le LPB spontané et celui médicamenteux. La liste des médicaments inducteurs, non exhaustive, est reportée sur le tableau 1.
Le délai moyen entre la prise médicamenteuse et l’apparition du lichen est de 165 jours (60-406) d’où la recherche systématique de médicaments inducteurs initiés dans les 6 mois avant le début du LPB(2). Très souvent, les patients sont polymédicamentés, d’où la difficulté d’identifier le médicament responsable. L’arrêt du traitement n’est pas indispensable en l’absence de symptômes gênants du LPB sous traitement local. Le délai de régression du LPB après arrêt du médicament inducteur peut être long de plusieurs mois.
La localisation des lésions lichéniennes en regard de matériaux de restauration dentaire, quelle que soit leur constitution, doit faire évoquer des lésions lichénoïdes induites de contact, dont l’histologie est similaire à celle d’un LPB spontané. La relation topographique peut être complète ou partielle, le traitement du lichen souvent peu efficace. Il est alors souhaitable de réaliser des tests épicutanés, associant une batterie standard européenne et une batterie spéciale des matériaux dentaires. En cas de tests positifs, seuls les patients avec un LPB symptomatique en relation topographique avec le matériel dentaire auront un changement de matériel dentaire, dont la nature sera guidée par les résultats des tests épicutanés.
ÉVOLUTION
Contrairement au lichen plan cutané, l’évolution du LPB est beaucoup plus souvent chronique qu’aiguë avec des poussées évolutives récidivantes. Ce fait doit être pris en compte dans le choix du traitement. Les poussées peuvent être déclenchées par le stress, certains aliments, des facteurs mécaniques (frottements d’appareil dentaire, restauration dentaire), des médicaments en particulier les anti-inflammatoires non stéroïdiens ; ces facteurs déclenchant seront évités si possible. Le risque de transformation en carcinome épidermoïde a été évalué différemment dans les différentes études, estimé à 1,42 % dans une synthèse bibliographique(3), survenant surtout dans les formes érosives ou atrophiques. Il est important d’expliquer au patient ce risque en précisant qu’il est faible, mais qu’il implique une surveillance au long cours au minimum une fois par an avec nécessité d’une consultation en cas d’apparition d’une lésion inhabituelle. L’étude finlandaise a comparé 13 100 femmes avec un diagnostic de lichen plan quelle que soit la topographie à toute la population ; 1 520 cancers ont été signalés (SIR 1,15 ; IC95 % 1,09-1,20) surtout de la langue (SIR 12,4 ; IC95 % 9,45-16,0), de la cavité buccale (SIR 7,97 ; IC95 % 6,79-9,24), des lèvres (SIR 5,17 ; IC95 % 3,06-8,16), mais aussi du larynx (SIR 3,47 ; IC95 % 1,13-8,10), de la vulve (SIR 1,99 ; IC95 % 1,18-3,13) et de l’œsophage (SIR 1,95 ; IC95 % 1,17-3,04)(4).
PRISE EN CHARGE
Règles générales
Une prise en charge initiale parodontale (conseils d’hygiène, détartrage) et dentaire (élimination des facteurs traumatiques) est recommandée du fait d’une amélioration des paramètres cliniques parodontaux, de la qualité de vie (douleurs, inconfort, gêne), de la sévérité clinique de la maladie. Le retentissement psychologique du LPB est parfois sévère, surtout dans les formes douloureuses, érosives, chroniques, génératrices de stress, dépression et anxiété, eux-mêmes facteurs déclenchant des poussées. Il doit être pris en compte dans le choix du traitement en association avec un éventuel suivi psychologique.
Traitements locaux
Seules les lésions gênantes justifient un traitement. Il existe un consensus sur le traitement de première intention consistant en une corticothérapie locale, dont l’efficacité a été démontrée dans de nombreuses études contrôlées. Les modalités de cette corticothérapie topique varient d’un malade à l’autre : bain de bouche, spray, crème, glossettes, pâte adhésive, injection lésionnelle. Aucun vecteur n’est idéal. La prednisolone (2 à 3 comprimés effervescents de 20 mg dilués dans un demi-verre d’eau), utilisée en bains de bouche 2 à 3 fois par jour a comme inconvénients un risque plus important d’absorption systémique et un faible temps de contact avec la muqueuse. Les dermocorticoïdes forts ou très forts peuvent être appliqués dans la bouche 2 fois par jour directement sur les lésions ; leur galénique n’est cependant pas adaptée à la cavité buccale. Pour augmenter leur adhésivité à la muqueuse, ils peuvent être inclus à partie égale dans une pâte adhésive (Orabase ®), inégalement supportée. La bétamethasone existe sous forme de glossette à une dose faible (0,1 mg/glossette) insuffisante dans les formes sévères. Le fluticasone propionate en spray est souvent mal toléré à long terme. Pour les lésions gingivales, il est possible d’utiliser des gouttières thermoformées permettant de main tenir les corticosteroïdes au niveau des lésions à traiter. Les candidoses constituent l’effet secondaire le plus fréquent des corticoïdes topiques ; elles peuvent être prévenues par l’utilisation d’antifongiques. Un risque d’absorption systémique lors des traitements longue durée est toujours possible, notamment en cas d’injections sous-lésionnelles de corticoïde à libération prolongée tel que l’acétonide de triamcinolone (Kénacort® retard : 40 mg), dans les formes réfractaires. La répétition de ces injections n’est pas recommandée du fait de ce risque systémique difficile à évaluer et des complications locales avec atrophie de la muqueuse.
De nombreux autres traitements locaux ont été évalués, souvent dans des essais contrôlés par rapport au placebo ou aux corticoïdes locaux, aucun n’ayant montré une supériorité par rapport aux corticoïdes locaux. La nécessité d’un recrutement suffisant oblige souvent malheureusement dans ces essais à inclure tous les malades sans limitation aux seuls cas de LPB réfractaires à une corticothérapie locale correctement suivie. Ils peuvent être utilisés en deuxième intention tels les immunosuppresseurs topiques (ciclosporine, tacrolimus, pimécrolimus, sirolimus). Actuellement en France, la préférence est donnée aux tacrolimus du fait d’une galénique disponible pour le revêtement cutané (Protopic®), utilisée dans la bouche deux fois par jour en cas de LPB non répondeur aux corticoïdes topiques ou avec une candidose récidivante induite par la corticothérapie.
Les rétinoïdes topiques sont réservés aux formes hyperkératosiques, mal supportés en cas d’érythème ou d’érosion. L’aloe vera topique ou autre nutraceutique (purslane, lycopène, curcumine par voie topique ou orale) peut avoir une efficacité comme un gel à l’acide hyaluronique 2 %, une pâte à 5 % d’amlexanox(5,6). La thérapie photodynamique, la PUVA-thérapie, certains lasers dont le laser Excimer se sont révélés efficaces dans certaines observations. Tous ces traitements permettent parfois d’éviter le recours à un traitement par voie générale dont aucun n’est satisfaisant.
Traitements systémiques
La prednisone (Cortancyl®) est efficace à une dose élevée (> 0,5 mg/kg/j), incompatible avec une administration prolongée ; comme les corticoïdes topiques, leur activité est essentiellement suspensive avec un risque de récidive voire de rebond à l’arrêt du traitement dont la durée ne doit pas dépasser 1 mois à forte dose.
Prolongée longtemps à une dose supérieure à 7,5 mg/j, la prednisone a des effets secondaires plus importants que les inconvénients induits par un LPB. L’adjonction d’immunosuppresseurs de type mycophénolate mofétil à la corticothérapie générale pourrait peut-être permettre sa décroissance sans rebond.
Comme les rétinoïdes topiques, les rétinoïdes par voie générale sont mal supportés en cas d’érythème ou d’érosion.
De nombreuses biothérapies (anti-TNF, anti-IL12-23, antiCD20, anti-IL17) ont été essayées avec des résultats initiaux parfois favorables, mais décevants au long cours. Il en est de même de l’aprémilast (Otezla®), du thalidomide, du ruxolitinib, des immunoglobulines à fortes doses en intraveineux.
Dans les LPB particulièrement sévères réfractaires, une photochimiothérapie extracorporelle peut être proposée avec les mêmes modalités que celles utilisées dans la réaction du greffon contre l’hôte(7) ; il s’agit d’une technique lourde justifiant une hospitalisation de jour initialement 2 fois par semaine ou 2 fois tous les 15 jours.
CONCLUSION
Le LPB est une maladie très hétérogène dans son expression clinique et son retentissement sur la qualité de vie. Le traitement est symptomatique et repose en première intention sur la corticothérapie locale, meilleur traitement en termes d’efficacité/effets secondaires. Les formes graves sont de traitement difficile, avec recours à des thérapies pouvant être dangereuses à long terme alors que le risque de transformation carcinomateuse est faible.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :