Publié le 13 oct 2021Lecture 5 min
La dermatite atopique, les progrès d’aujourd’hui ouvrent la voie pour demain
Denise CARO, Boulogne-Billancourt
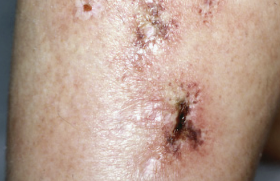
La dermatite atopique (DA) est un motif fréquent de consultation chez l’enfant et chez l’adulte. Son incidence a été multipliée par 2 ou par 3 les trente dernières années(1). Les progrès récents dans la compréhension clinique et physiopathologique de la maladie permettent d’affiner les stratégies thérapeutiques, notamment en ciblant les voies inflammatoires impliquées dans les différentes formes de la maladie.
Selon les recommandations publiées en 2018, la prise en charge de la DA doit être graduée en fonction de la sévérité de la maladie. L’éventail des traitements proposés dans les formes sévères est en train de s’élargir(2). Jusqu’à récemment, un seul traitement systémique, la ciclosporine, avait une AMM dans la DA. D’autres comme le méthotrexate étaient prescrits sans avoir l’indication.
L’arrivée d’une première biothérapie anti-IL-4/IL-13, le dupilumab, a révolutionné le traitement des formes sévères. Efficace et bien toléré, il a changé l’adhésion des patients à leur traitement. Selon une étude espagnole, 20 mois après initiation du traitement, 93,6 % des patients poursuivent le dupilumab, alors que c’est le cas de seulement 36,7 % avec la ciclosporine et de 32,1 % avec le méthotrexate(3). Cette première innovation a ouvert la voie au développement de nouvelles approches thérapeutiques fondées sur la physiopathologie.
Une multitude de cytokines impliquées
Au cours de la DA, l’altération de la barrière cutanée facilite la pénétration de molécules qui activent les kératinocytes et entraînent la production d’alarmines (IL-1ß IL-25, IL-33, TSLP). Ces signaux de danger déclenchent la production de cytokines pro-inflammatoires Th2 (IL-4, IL- 5 et IL-13 IL-31). On sait que les voies Th22, Th1 et Th17 sont également impliquées avec des contributions variables en fonction du phénotype de la maladie. Enfin, l’inflammation est à l’origine du prurit, dont le grattage aggrave l’inflammation et enclenche un cercle vicieux. Dès lors, deux approches thérapeutiques sont possibles : soit on cible sélectivement une (voire 2) des cytokines impliquées dans la DA (comme le dupilumab anti-IL4/IL13), soit on intervient en amont en inhibant les Janus Kinase (JAK).
En effet, les JAK transmettent les signaux induits par les cytokines au noyau, via la phosphorylation et l’activation de facteurs de transcription STAT. Ainsi, l’inhibition de la voie des JAK permet de cibler plusieurs cytokines clés dans la DA (IL-13, TSLP, IL-4, IL-13, IL-31 et IL-33) ; ce qui laisse espérer une réponse thérapeutique large, quel que soit le type de lésions. De nombreuses molécules en développement dans la DA sont dans les pipelines. Parmi les plus prometteuses, trois molécules ciblant des interleukines et trois inhibiteurs de JAK (JAKi).
L’anti-IL13, lebrikizumab, a été comparé à un placebo, associé à un dermocorticoïde (DC), dans un essai de phase 2. À 12 semaines, 55 % des patients sous lebrikizumab avaient atteint un EASI-75 vs 34 % dans le groupe placebo; p < 0,05)(4) . Un autre anti-IL13, le tralokinumab, a également été comparé à un placebo, en association avec un DC, dans une étude de phase 3. À 16 semaines, 56 % des patients du groupe anti-IL13 avaient un EASI-75 vs 36 % dans le groupe placebo. La tolérance était bonne, avec un peu plus de conjonctivites dans le groupe principe actif(5).
Enfin, l’efficacité sur le prurit d’un anti-IL31, le nemolizumab, a été évaluée, en association avec un DC, chez des patients avec une DA sévère. À 16 semaines, le score de prurit (NRS) était significativement plus bas dans le groupe anti-IL31(6).
Une nouvelle classe thérapeutique
Trois JAKi sont à un stade avancé de développement dans la DA (essais phase 3). L’un d’eux, le baricitinib, vient d’obtenir son AMM dans cette indication. Breeze-AD7 a montré la supériorité du baricitinib (inhibiteur JAK-1 et 2) au placebo, en association avec un DC. À 16 semaines 50 % des patients baricitinib avaient un EASI-75 vs 23 % dans le groupe placebo. Parmi les répondeurs 44 % des patients baricitinib n’utilisaient plus de DC vs 16,2 % du groupe placebo(7).
Dans ces essais, la tolérance du baricitinib était bonne. Aucun événement grave n’a été signalé. Il y avait un peu plus d’herpès avec le JAKi (8) L’abrocitinib est un inhibiteur JAK-1 qui permet 61 % d’EASI-75 à 12 semaines en monothérapie vs 10 % dans le groupe placebo. La tolérance a été estimée bonne avec quelques effets secondaires peu graves (nausées, acné, herpès)(9).
Enfin, l’upadacitinib (UPA), inhibiteur JAK-1, a fait preuve d’une bonne efficacité en monothérapie dans un essai de phase 3 (UPA 15 mg, 30 mg ou placebo), avec à 16 semaines 80 % d’EASI-75 dans le groupe UPA 30 mg (vs 16 % avec le placebo) et 62 % d’IGA de 0 ou 1 avec UPA 30 mg (vs 8,2 % placebo) (p < 0,01). 60 % des patients UPA 30 mg avaient amélioré de plus de 4 points leur score de prurit (vs 9 % placebo). Le soulagement était rapide, avec une différence significative dès la première semaine. Aucun effet secondaire grave ni anomalie biologique n’ont été signalés ; comme avec les autres JAKi, des cas d’acné ont été observés(10).
Des essais avec des comparateurs actifs débutent. Une étude de phase 3 (dont l’objectif n’était pas de montrer la supériorité de l’un ou de l’autre traitement) a comparé 2 doses d’abrocitinib au dupilumab, en association à un DC. À 16 semaines, il y avait 60 % d’EASI-75 dans le groupe abrocitinib 100 mg, 71 % dans le groupe abrocitinib 200 mg, 65,5 % dans le groupe dupilumab et 31 % dans le groupe placebo.
Les auteurs ont noté une réponse plus rapide sur le prurit (dès la 2e semaine) avec le JAKi qu’avec l’anti-IL14/IL13. Sur le plan de la tolérance, il n’y a pas eu d’effets secondaires sévères ; il y avait un peu plus de conjonctivites avec le dupilumab et un peu plus d’acné et de nausées avec l’abrocitinib(11).
Le lancement d’études comparant l’upadacitinib et le dupilumab devrait permettre d’en apprendre davantage sur la place respective de ces deux classes thérapeutiques dans la DA. Il semble d’ores et déjà que les JAKi agissent plus vite que les biothérapies qui ont un effet plus durable. Quoi qu’il en soit, l’élargissement des options thérapeutiques permettra de mieux répondre aux besoins des patients dont les formes de DA sont hétérogènes.
D’après un symposium organisé par les laboratoires AbbVie avec la participation de Marie-Aleth Richard (Marseille), Ziad Reguiaï (Reims), Audrey Nosbaum (Lyon) et Sébastien Barbarot (Nantes)
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :