Cancérologie
Publié le 10 mai 2017Lecture 5 min
Prise en charge des mélanomes aux stades ganglionnaire et métastatique
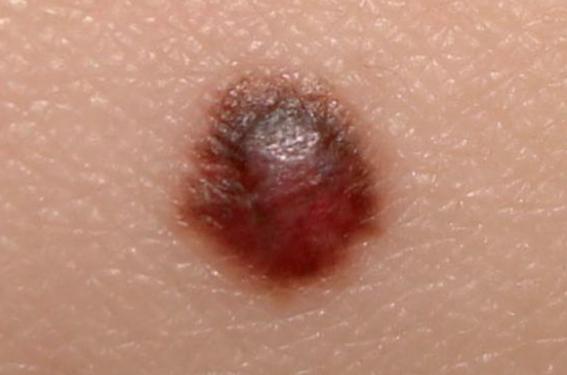
L’interféron (IFN), utilisé à faible dose dans les mélanomes de > 1,5 mm ou en stade IIa, ou à fortes doses, risque d’être rapidement dépassé par l’arrivée des nouveaux traitements qui ont montré leur efficacité dans les stades métastatiques.
Un essai EORTC ayant testé l’ipilimumab (anti-CTLA-4) à la dose de 10 mg/kg en induction, puis en traitement d’entretien tous les 3 mois pendant 3 ans ou jusqu’à progression, a en effet montré une réduction de 25 % du risque de récidive avec une nette et rapide séparation des courbes de survie sans récidive, au prix toutefois d’une toxicité non négligeable.
Reste à savoir si l’efficacité de ce check-point inhibiteur peut être démontrée en situation adjuvante, indication que vient d’approuver la FDA.
Concernant les traitements couramment utilisés au stade ganglionnaire, il a été montré que les fortes doses intermittentes d’IFN, visant à diminuer les effets secondaires, sont significativement moins efficaces que les fortes doses en situation adjuvante sur les micrométastases ou les macrométastases. La radiothérapie des sites de curage diminue les récidives dans le site opératoire sans modifier la survie et au prix d’une aggravation du lymphœdème.
Quelle est la bonne cible des traitements adjuvants ?
Selon les données du registre nord-américain SEER, ce sont les mélanomes à faible risque en stades Ia, IIb-IIc qui fournissent le plus gros contingent de tumeurs métastatiques ; les tumeurs de < 1 mm seraient responsables d’environ 30 % des décès par mélanome. Le nombre élevé de ces tumeurs, individuellement à faible risque, explique leur forte contribution et en fait la cible des nouvelles thérapies. Encore faut-il mieux comprendre la maladie résiduelle. Cette phase dormante, sous contrôle du système immunitaire, peut se réactiver très longtemps après la tumeur primitive. La maladie n’est pas localisée seulement dans le ganglion sentinelle, dont la résection n’améliore pas la survie. Les modèles animaux ont montré que la croissance tumorale est contrainte tant que l’immunité innée est efficace contre les cellules dormantes.
Il est donc probable que les thérapies adjuvantes devraient être administrées précocement à un stade où l’immunité innée est encore efficace, pour contribuer à l’éradication des cellules dormantes.
La meilleure preuve de validité de ce concept vient de la démonstration d’une meilleure efficacité de l’interféron et de l’ipilimumab chez les patients sans macrométastases. La survenue d’une ulcération en réponse au traitement serait un gage d’efficacité, signant une réaction immunologique forte.
Plusieurs traitements adjuvants sont évalués à ce stade.
Deux essais sont en cours avec un BRAF-inhibiteur, seul ou associé à un MEK-inhibiteur, chez des patients porteurs d’un envahissement macroganglionnaire, ce qui n’est sans doute pas la phase la plus favorable pour intervenir ni la meilleure cible en santé publique. Les check-point bloqueurs font également l’objet d’essais. L’ipilimumab (anti-CTLA-4) possède toutefois un profil de toxicité peu favorable et, là encore, la cible choisie est la maladie macroganglionnaire qui n’est pas la meilleure en santé publique. Les anti-PD1 exerceraient peut-être un effet antitumoral direct et ont un profil de toxicité bien meilleur, permettant leur utilisation sur de plus larges populations. Leur activité dépend toutefois du maintien d’un site tumoral ; or, les essais cliniques sont appliqués chez des patients ayant eu une exérèse du ganglion sentinelle, voire un curage.
Nous attendrons les preuves d’efficacité des check-point bloqueurs en situation adjuvante, avant de crier victoire.
Les thérapies ciblées dans le mélanome métastatique
La première stratégie consiste à bloquer BRAF et MEK, près de la moitié des patients étant porteurs de mutations de BRAF V600.
En 2015, le traitement s’oriente plutôt vers des bithérapies. Les données les plus récentes montrent, en effet, l’émergence de résistance aux monothérapies, très souvent liées à des réactivations de la voie des MAP kinases, et l’extrême variabilité des réponses interindividuelles et même intra-individuelles selon le site métastatique. La mise en évidence de réactivation de la voie des MAP kinases donne du sens à une bithérapie d’emblée associant un BRAF-inh et un MEKinh d’emblée.
Plusieurs essais de phase 3 testent cette combinaison, notamment COMBI-d (dabrafénib + tramétinib versus dabrafénib) et COMBI-v (dabrafénib + tramétinib versus vémurafénib). Ces essais montrent des taux de réponses objectives équivalents pour les deux essais, avec une augmentation de la survie globale d’environ 30 %, 10 % de patients en réponse complète et une médiane sans progression passant à 9-10 mois. L’objectif sera d’obtenir 50 % de patients vivants à 2 ans, alors qu’aujourd’hui ces nouveaux traitements permettent 74 % de patients vivants à 1 an.
Une analyse poolée rassemblant tous les patients traités en bithérapie (dans les essais précités et les phase 1) montre une médiane de survie entre 25 et 26 mois et laisse espérer que certains patients seront définitivement contrôlés. Cette analyse a aussi évalué les facteurs associés à une meilleure survie. Le taux de LDH apparaît comme un facteur déterminant : un taux > 2N est associé à une probabilité d’évolution favorable 4 fois plus basse, comparativement à un taux de LDH normal. La survie sans récidive et la survie globale sont non seulement impactées par le taux de LDH, mais par le statut ECOG, le nombre de sites métastatiques et la localisation de ces derniers. Il est probable que la bithérapie ciblée ne soit pas le meilleur traitement chez les patients avec LDH élevées.
Des résultats comparables sont observés dans l’essai coBRIM avec l’association cobimétinib + vémurafénib, avec toutefois un profil d’effets indésirables différent (moins de fièvre, mais davantage de phototoxicité et de diarrhée ainsi qu’une élévation des transaminases).
D’autres thérapies ciblées sont en cours de développement (encorafénib, binimétinib), dont l’efficacité serait du même ordre de grandeur avec un profil de tolérance meilleur, sans phototoxicité ni fièvre.
Pour aller au-delà de ces bithérapies ciblées, se pose aussi la question de leur combiner un immunomodulateur.
Les immunomodulateurs au stade métastatique
La deuxième stratégie utilisée est indépendante des mutations de BRAF et fait appel aux check-point inhibiteurs : des anticorps monoclonaux anti-CTLA-4 (lymphocyte- T cytotoxique associé à la protéine 4, molécule co-inhibitrice du système immunitaire), tel ipilimumab, ou anti-PD-1 (dirigé contre la protéine PD-1, récepteur coinhibiteur des cellules T), tels le pembrolizumab et le nivolumab. Ces molécules ont fait l’objet de nombreuses études prometteuses.
D’après « Mélanome : le point en pratique après 5 ans de progrès » avec la participation de P. Saiag, B. Dreno et J.-J. Grob – JDP 2016
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :