Congrès
Publié le 31 mar 2020Lecture 8 min
Aller plus loin dans la prise en charge du mélanome
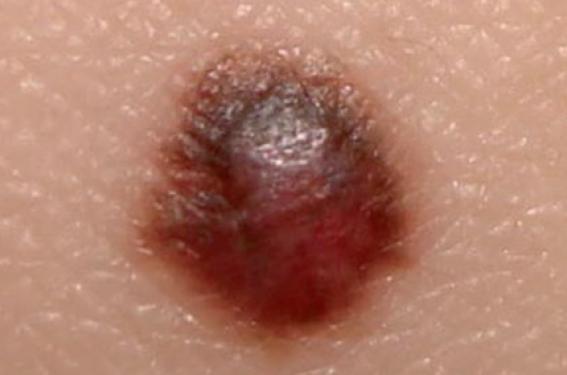
La prise en charge du mélanome a connu une évolution fulgurante depuis 2011. Thérapies ciblées et immunothérapie représentent deux stratégies différentes : la thérapie ciblée donne des résultats très rapides alors que l’immunothérapie agit plus lentement, mais se distingue par le maintien de la réponse thérapeutique. Il est possible de raisonner en termes d’efficacité (survie sans progression) et d’acceptabilité (inverse de la toxicité), le traitement optimal visant à une grande efficacité et une grande acceptabilité. Dans cette approche, l’anti-PD-1 a le meilleur rapport efficacité/acceptabilité.
Derniers résultats en survie
Le traitement combiné dabrafénib/tramétinib donne à 5 ans une survie globale de 34 %, une survie sans progression de 19 %, avec de meilleurs résultats lorsque les LDH sont normaux et des sites moins nombreux, mais 43 % d’effets secondaires grades 3/4, ce qui pose quotidiennement à l’oncologue la question de l’arrêt du traitement. L’immunothérapie par anti-PD-1 donne une survie globale de 34 % et une survie sans progression de 21 % à 5 ans, avec de meilleurs résultats en 1re ligne (41 % et 29 % respectivement) et moins d’effets secondaires graves (17 % de grades 3/4). Avec la combinaison anti-PD-1 + anti-CTLA4, la survie globale et la survie sans progression sont de 52 % et 36 %, quel que soit le statut BRAF, mais les effets secondaires sont plus fréquents (59 % de grades 3/4).
Les progrès concernent aussi les traitements adjuvants et néoadjuvants, avec soit des molécules seules anti-CTLA-4, anti-PD1, soit des associations. L’ipilimumab permet une survie sans progression de 41 % vs 30 % sous placebo à 5 ans. Le nivolumab permet de gagner 12 % comparativement à l’ipilimumab à 2 ans. La combinaison dabrafenib + tramétinib donne une survie sans progression de 58 % (vs 39 % sous placebo) à 3 ans, et le pembrolizumab de 71,4 % (vs 53,2 % sous placebo) à 2 ans. Le pourcentage de réponses sur la survie sans progression n’est pas encore connu.
Les enjeux futurs consistent à identifier trois groupes de patients : en résistance primaire, en résistance secondaire et non répondeurs. Un autre enjeu est celui des traitements combinés ou séquentiels ; vaut-il mieux s’orienter vers une approche allant d’une thérapie ciblée, qui va modifier l’expression de certains marqueurs et fournir un terrain favorable à l’immunothérapie ?
Il faut identifier des sujets répondeurs et des sujets à risque d’effets secondaires : on sait aujourd’hui que plus il y a de TIL (tumor infiltrating lymphocytes) dans l’environnement tumoral, meilleure est la réponse ; on travaille aussi sur la charge mutationnelle du mélanome, l’expression de néoantigènes étant associée à une possibilité de meilleure réponse, ainsi que sur le rôle potentiel du microbiome intestinal dans la sélection des patients répondeurs. Des marqueurs sanguins ont été identifiés (LDH, CRP, ADN circulants) ainsi que grâce au PETscan.
Quelle est la pertinence du ganglion sentinelle et du curage ganglionnaire ?
Le ganglion sentinelle (GS) a un intérêt pronostique, mais son ablation ne confère aucun bénéfice. La micrométastase peut être de topographie variable dans le ganglion et de diamètre variable, avec un effet-dose certain (la survie est équivalente si le ganglion mesure < 0,1 mm ou s’il n’y a pas de GS). Trois essais (MSLT-I, MSLT-II et DeCOG-SLT) n’ont pas montré de bénéfice du curage ganglionnaire en survie sans métastase à distance ou en survie globale ; en revanche cette pratique a une morbidité (jusqu’à 20 % de lymphœdème). Il n’est donc plus recommandé de faire de curage ganglionnaire systématique.
La décision de faire un GS (à visée pronostique) est basée sur deux critères. Chez les patients au-delà de T1B, le pronostic est clairement différent en présence d’un ganglion sentinelle, si bien que la recommandation actuelle est de proposer ce geste chez les patients ayant un Breslow de ≥ 1 mm, et de le discuter pour un Breslow entre 0,8 et 1 mm ou un mélanome de 0,8 mm ulcéré. Les facteurs de risque associés à la positivité du ganglion sentinelle sont l’épaisseur, l’âge jeune (< 40 ans) et le sexe masculin.
Pourtant, la nouvelle version de la classification AJCC 8, assez complexe, repose sur le nombre de ganglions atteints, le Breslow, l’existence ou non d’ulcération. Sachant qu’il n’est plus recommandé de faire un curage ganglionnaire, on peut s’interroger sur l’apport de cette nouvelle classification. La reclassification des patients AJCC 7 en AJCC 8 se traduit par une redistribution des patients entre les stades IIIA à IIID. Le pronostic n’est pas tout à fait le même pour tous les patients classés en IIIA selon AJCC 7 ; il diffère s’il existe des micrométastases de < 1 mm avec une survie à 5 ans de 91 % ou de > 1 mm avec une survie à 5 ans de 72 %.
Les données en sous-groupe de l’essai KEYNOTE 054 avec le pembrolizumab montrent qu’avec la classification AJCC 7, les groupes traités vs placebo étaient bien séparés alors qu’avec une reclassification AJCC 8, le doute persiste quant à l’intérêt d’un traitement adjuvant dans les IIIA chez les patients ayant des micrométastases < 1 mm en raison des effets secondaires potentiels pour un bénéfice incertain. Quant aux IIIA mutés BRAF, la différence entre traitement adjuvant et pas de traitement semble persister.
Pour les stades II, la reclassification AJCC 8 génère des stades II de pronostic aussi mauvais que des stades III. On attend les résultats d’un procédé de classification, moins morbide que le GS, basé sur des signatures transcriptomiques (11 gènes/31 gènes) qui permettrait de définir, parmi les stades II voire les stades III, des patients à haut risque de rechute. Pour l’heure, le GS — comme l’AJCC — reste un outil imparfait mais incontournable pour décider du traitement adjuvant.
Quels traitements pour quels patients en situation adjuvante ?
En situation adjuvante, la qualité de vie prend un relief particulier.
Les essais n’ont pas montré de différence d’efficacité de l’immunothérapie en adjuvant stade III en fonction du statut BRAF. Il y a encore besoin de recul pour évaluer le bénéfice réel sur la survie globale des traitements adjuvants. À 4 ans de suivi, la survie sans rechute est de 67 % dans le bras dabrafénib + tramétinib de l’étude COMBI-AD vs 58 % dans le bras placebo, la survie sans métastase à distance de 64 % vs 56 %, la fréquence estimée de guérison est de 54 % vs 37 %.
Quel traitement adjuvant choisir ? Le nivolumab est indiqué en monothérapie dans le traitement adjuvant des patients ayant un mélanome avec atteinte des ganglions lymphatiques ou une maladie métastatique et ayant subi une résection complète. Le pembrolizumab est indiqué en monothérapie dans le traitement des patients atteints de mélanome stade III avec atteinte ganglionnaire ayant eu une résection complète. L’association dabrafénib + tramétinib est indiquée dans le mélanome stade III en cas de mutation BRAF V600.
Le choix dépend du profil du patient : ganglion locorégional identifié sur examen clinique, imagerie ou cytoponction, curage ganglionnaire positif, bilan d’extension négatif ; ganglion sentinelle positif, bilan d’extension négatif ; maladie métastatique ayant subi une résection complète.
Si le patient est BRAF+, le choix est entre anti-BRAF+MEK et immunothérapie anti-PD-1, à discuter dans une approche bénéfice/risque en fonction des comorbidités et de l’âge.
Si le patient est BRAF-, la seule alternative est l’immunothérapie anti-PD-1.
La thérapie ciblée en 1re ligne en adjuvant aura un bénéfice plus prononcé la 1re année ; le profil de tolérance est bon mais il y a davantage de rechutes à l’arrêt du traitement.
L’immunothérapie en 1re ligne se caractérise par un maintien du bénéfice dans le temps ; son efficacité n’est pas liée au statut BRAF ; les effets secondaires auto-immuns sont prolongés.
Chez un patient qui rechute sous traitement adjuvant ou dans les 3 mois suivant son arrêt :
Si le patient est BRAF+, après un premier traitement anti-PD-1, on peut débuter une thérapie ciblée anti-BRAF+MEK, ou continuer l’anti-PD-1 ou faire une chimiothérapie.
Si le patient est BRAF+ et que le premier traitement était une thérapie ciblée, on peut débuter une immunothérapie ou une chimiothérapie.
Si le patient est BRAF-, on peut débuter une immunothérapie combinée anti-CTLA-4 + anti-PD-1, ou continuer un antiPD-1, voire discuter une chimiothérapie.
Il est donc important pour définir la stratégie thérapeutique de disposer des bons éléments de choix : ganglion sentinelle, curage ganglionnaire, état général, nombre de sites métastatique, masse tumorale, rapidité de la rechute, et critères biologique (mutation BRAF, taux de LDH). Dans tous les cas, en situation adjuvante un élément majeur est de maîtriser les effets secondaires qui sont très variés, imprévisibles (pas de marqueurs prédictifs), avec une cinétique bien définie (survenue dans les 3 premiers mois et possibilité de reprendre le traitement après une interruption). Le patient doit être considéré comme un acteur de son traitement ; il participe au choix (mode d’administration per os ou IV, durée du traitement, bénéfice attendu, priorités du patient, effets secondaires, retentissement sur la qualité de vie).
En situation métastatique, quels critères prendre en compte ?
Aujourd’hui, il existe deux axes thérapeutiques, l’immunothérapie et les thérapies ciblées. En monothérapie, l’ipilimumab n’est pas disponible mais il existe des données montrant la supériorité de l’anti-PD-1.
Aucun argument ne permet de différencier le pembrolizumab et le nivolumab hormis les schémas d’admini stration (toutes les 3 ou 6 semaines vs toutes les 2 ou 4 semaines respectivement). La vraie question concerne le choix entre monothérapie et bithérapie, en l’absence d’essai comparatif de phase 3.
L’essai qui offre le plus d’arguments pour évaluer ces stratégies est CheckMate 067 comparant nivolumab + ipilimumab vs nivolumab vs ipilimumab ; il ne fournit pas cependant d’argument décisif faute de puissance statistique suffisante. En survie sans progression et en survie globale, la bithérapie fait mieux que le nivolumab, alors que l’ipilimumab semble loin derrière ces deux comparateurs. La survie globale à 5 ans dépasse aujourd’hui 50 %. Le statut BRAF n’a pas d’impact sur les résultats, pas plus que le statut PD-L1.
À 5 ans, la majorité des patients ayant reçu un traitement combiné pour un mélanome métastatique sont sans traitement. Toutefois, il existe clairement des problèmes de toxicité, plus de 50 % des patients développant des toxicités sévères sous combinaison thérapeutique (vs 15-25 % sous monothérapie).
Sous nivolumab ou ipilimumab, la principale raison d’arrêt de traitement est la progression de la maladie, sous traitement combiné, c’est la toxicité du traitement. L’utilisation de schémas allégés pourrait limiter les effets secondaires.
Dans le cas particulier des métastases cérébrales, deux essais concordants montrent un taux de réponse très élevé (> 50 %) avec la combinaison nivolumab + ipilimumab. En pratique, la combinaison ipilimumab + nivolumab n’est admise au remboursement qu’en 1re ligne de traitement dans le mélanome avancé, chez des patients en bon état général, BRAF non mutés, sans métastase cérébrale active. Elle doit administrée dans des centres ayant l’expertise de la gestion de ce traitement et de sa toxicité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :