Publié le 20 avr 2010Lecture 11 min
Diagnostic et traitement du mélanome : recommandations européennes
F. AUBIN, Service de dermatologie, CHU de Besançon
Ces recommandations ont été rédigées par la Fondation européenne de dermatologie (EFD), l’Association européenne de dermato-oncologie (EADO) et l’Organisation européenne pour la recherche et le traitement du cancer (EORTC).
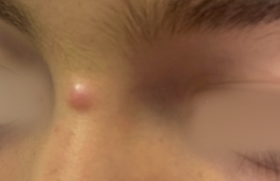
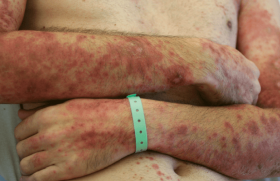
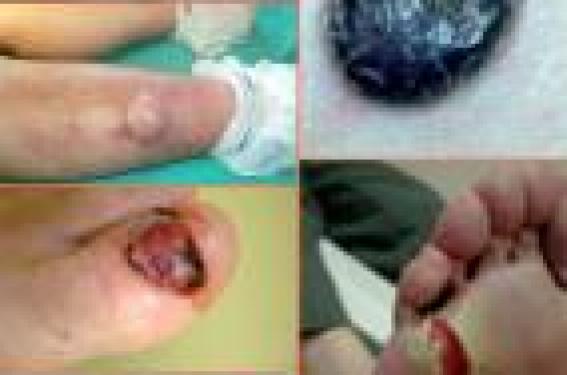
Le mélanome est une tumeur maligne qui se développe à partir des mélanocytes, le plus souvent cutanés, et plus rarement à partir des tissus oculaires (uvée, conjonctives et corps ciliaires) ou méningés ou des muqueuses. Le plus souvent, il s’agit de tumeurs pigmentées, mais elles peuvent aussi être achromiques. Le mélanome est responsable de 90 % des décès par cancers cutanés. Épidémiologie L’incidence du mélanome augmente régulièrement dans le monde, en particulier chez les sujets de phototype clair, ayant reçu une exposition solaire intense dans l’enfance. L’incidence annuelle en Europe du Sud varie entre 6 et 10 pour 100 000 personnes, atteint 10 à 14 pour 100 000 en Europe centrale, 10 à 25 pour 100 000 aux États-Unis et 50 à 60 pour 100 000 en Australie. Cinq à 10 % des mélanomes se développent dans un contexte familial, mais le plus souvent il s’agit de patients présentant de multiples lésions næviques plus ou moins atypiques. En dehors de ces facteurs constitutionnels et génétiques, le facteur environnemental le plus connu reste l’irradiation ultraviolette intense et intermittente, en particulier pendant l’enfance. Aspects anatomo-cliniques Quatre différents types cliniques et histologiques de mélanomes sont identifiés : – mélanome à extension superficielle ; – mélanome nodulaire ; – mélanome lentigineux ; – mélanome lentigineux acral. D’autres sous-types de mélanomes sont différenciés : mélanome desmoplastique, mélanome amélanotique, mélanome polypoïde, qui constituent environ moins de 5 % des cas. Dans plus de 90 % des cas, le mélanome est diagnostiqué au stade de tumeur primitive, sans métastase. La survie à 10 ans varie alors entre 75 et 85 %. Figure 1. Différentes formes cliniques de mélanome cutané primitif. Les principaux facteurs pronostiques pour le mélanome primitif sans métastase sont : – l’épaisseur tumorale (indice de Breslow) ; – la présence ou non d’une ulcération macro- ou microscopique ; – l’activité mitotique ; – le niveau de Clark, en particulier pour les mélanomes inférieurs à 1 mm. La dissémination loco-régionale s’exprime par : – des micro-métastases identifiées dans le ganglion de drainage par la biopsie du ganglion sentinelle ; – des métastases satellites de la tumeur primitive (inférieures dans un rayon de 2 cm) ; – des métastases en transit au-delà de 2 cm de la tumeur primitive et avant le premier ganglion de drainage ; – des métastases ganglionnaires palpables régionales. La survie à 10 ans pour les patients présentant des micro-métastases atteint 30 à 70 %, 30 à 50 % pour les patients avec des métastases satellites ou en transit et 20 à 40 % pour les patients présentant des métastases ganglionnaires régionales. L’extension à distance du territoire de drainage, sous la forme de métastases cutanées, souscutanées, ganglionnaires ou viscérales s’accompagne d’une survie médiane de 6 à 9 mois, selon le taux de LDH. Diagnostic Le diagnostic du mélanome est le plus souvent clinique, basé sur les critères A, B, C, D et E d’une lésion pigmentée. La sensibilité diagnostique des dermatologues est d’environ 70 %. La dermoscopie réalisée par des dermatologues expérimentés permet d’augmenter la sensibilité à 89 % avec une spécificité de 79 %. La sensibilité diagnostique des dermatologues est d’environ 70 %. Diagnostic histologique Le compte-rendu histologique d’un mélanome cutané doit comporter le diagnostic, le type anatomo- clinique, l’épaisseur tumorale, la présence ou l’absence d’ulcération épidermique, le niveau d’invasion (niveau de Clark), en particulier pour les mélanomes inférieurs à 1 mm d’épaisseur, la présence ou non de micro-métastases satellites et la dimension des marges d’exérèse latérale et en profondeur. Figure 2. Aspect dermoscopique de mélanome. D’autres informations peuvent être également fournies : – le nombre de mitoses/mm2 ; – le type de croissance (verticale ou horizontale) ; – l’existence ou non d’une régression tumorale ; – l’existence ou l’absence d’un infiltrat lymphocytaire dense ; – la présence ou non d’embolies lymphatiques ; – l’atteinte vasculaire ou périneurale. L’examen histologique peut être complété par une étude immunohistochimique (protéine S100, HMB 45, Melan- A), afin de confirmer la nature mélanocytique de la lésion tumorale. Bilan d’extension Celui-ci n’est pas recommandé chez les patients à faible risque, bien que la définition des patients à faible risque varie d’un centre à l’autre. S’il est réalisé, le bilan d’extension doit comporter une échographie des aires ganglionnaires régionales, une radiographie pulmonaire et une échographie abdomino-pelvienne. Chez les patients à haut risque, le bilan peut être complété par un scanner et/ou un Pet-scan et/ou une IRM selon les indications cliniques. Les taux sériques de LDH et de protéine S 100 peuvent être également utilisés comme facteurs pronostiques. Évaluation du ganglion sentinelle L’évaluation du ganglion sentinelle a un intérêt pronostique. Aucun intérêt thérapeutique, en particulier sur la survie n’a actuellement été démontré. L’évaluation du ganglion sentinelle n’est pas très bien standardisée, bien que la plupart des centres effectuent une analyse histologique et immunohistochimique. L’expérience du centre d’anatomopathologie est primordiale. L’évaluation du ganglion sentinelle n’est pas recommandée pour les mélanomes inférieurs à 1 mm en raison du très faible taux de micro-métastases. Cependant, elle peut être réalisée s’il y a d’autres facteurs histologiques de mauvais pronostic (niveau IV, ulcération, etc.). L’évaluation du ganglion sentinelle n’est pas recommandée pour les mélanomes inférieurs à 1 mm. Lorsque l’évaluation du ganglion sentinelle est négative, il n’est pas nécessaire d’effectuer de curage ganglionnaire complémentaire. En cas de micro-métastases ganglionnaires sur le ganglion sentinelle, aucune étude n’a montré que le curage ganglionnaire complémentaire augmentait la survie. Lorsqu’il est effectué, ce curage ganglionnaire complémentaire montrera des ganglions métastatiques dans 5 à 12 % des cas. Le curage ganglionnaire complémentaire peut être remplacé par une surveillance échographique et actuellement une étude compare la surveillance échographique ganglionnaire après évaluation du ganglion sentinelle avec le curage ganglionnaire complémentaire. Traitement Traitement chirurgical du mélanome cutané primitif Le traitement chirurgical reste le traitement de première intention du mélanome. Plusieurs études ont montré que les biopsies intratumorales de mélanome ne modifient pas les pronostics par rapport aux biopsies exérèses complètes initiales. L’excision chirurgicale élargie doit être réalisée dans un délai de 4 à 6 semaines après le diagnostic histologique initial. Des marges d’exérèse élargie sont recommandées en fonction de l’épaisseur tumorale : – mélanome in situ : marges de 0,5 cm ; – mélanome inférieur à 2 mm : marges de 1 cm ; – mélanome supérieur à 2 mm : marges de 2 cm. Il semble que le respect de ces marges ait un impact sur les récidives loco-régionales, mais il n’y a aucune étude montrant l’impact des marges d’exérèse sur la survie globale. Les lentigos malins du visage doivent faire l’objet d’une chirurgie respectant les aspects fonctionnels et esthétiques de la face. La radiothérapie ou l’application d’imiquimod sont des alternatives efficaces. Cependant, le patient doit être informé de l’absence d’évaluation histologique de ces traitements. Figure 4. Métastase de mélanome. Les mélanomes acraux et muqueux doivent faire l’objet d’une exérèse complète avec si possible une marge de sécurité d’au moins 1 cm, bien qu’il y ait peu d’études sur ce sujet. Traitement chirurgical des métastases ● Métastases ganglionnaires : le curage ganglionnaire complet est recommandé. ● Métastases cutanées : le traitement recommandé est la chirurgie. En cas de lésions multiples monoméliques, la chimiothérapie hyperthermique monomélique par melphalan ± TNF-alpha peut être utilisée. D’autres traitements destructeurs (cryothérapie, laser) ou immunomodulateurs (imiquimod, interféron alpha) peuvent être utilisés. ● Métastases viscérales : en cas de métastase unique, la chirurgie est le traitement de choix. Radiothérapie Le mélanome est une tumeur peu radiosensible. La radiothérapie peut être indiquée pour les lentigos malins du visage, en cas de contre-indication chirurgicale. La radiothérapie peut être également proposée en cas d’exérèse ganglionnaire ou de métastase cutanée insuffisante sur le plan chirurgical. La radiothérapie prophylactique des aires ganglionnaires de drainage n’est pas recommandée. La radiothérapie des métastases osseuses peut être proposée, à titre palliatif (effet antalgique, effet antiinflammatoire, risque de compression médullaire). La principale indication de la radiothérapie dans le mélanome reste les métastases cérébrales, qui s’accompagnent d’une espérance de vie de 3 à 5 mois. Elle améliore la symptomatologie douloureuse et neurologique dans 50 à 70 % des cas. Elle doit être associée à une corticothérapie systémique. La radiothérapie stérotaxique à dose unique (gamma knife) ne s’adresse qu’aux lésions uniques ou peu nombreuses (inférieures à 3) et de petite taille (inférieure à 3 cm). Traitement adjuvant Le traitement adjuvant s’adresse aux patients sans maladie résiduelle, mais à haut risque de récidive loco-régionale ou systémique. La chimiothérapie systémique ou monomélique n’a jamais démontré d’efficacité adjuvante dans le mélanome. Immunothérapie adjuvante par interféron Il existe actuellement deux schémas de traitement par interféron dans le mélanome en adjuvant : – pour les mélanomes supérieurs à 1,5 mm d’épaisseur, l’interféron peut être utilisé à faible dose (3 millions d’unités par semaine pendant 18 mois) pour les mélanomes supérieurs à 1,5 mm d’épaisseur. Seules deux études ont montré une augmentation significative de la survie sans récidive. Dans une étude, il existait une tendance non significative vers une survie globale prolongée ; – pour les mélanomes de stade III : l’interféron a été utilisé à différentes doses, mais en général à des doses beaucoup plus élevées selon le schéma de Kirkwood. Seules deux études prospectives et randomisées ont montré une prolongation de la survie sans récidive et une seule étude de la survie globale. Plus récemment, une forme pégylée d’interféron alpha a montré un effet significatif sur la survie sans récidive chez tous les patients et en particulier, chez les patients avec micro-métastases (N1). Aucun effet sur la survie globale n’était démontré dans cet essai. Après plus de 10 ans d’études, la prescription d’interféron en adjuvant dans le mélanome fait toujours l’objet de discussions. S’il existe un bénéfice en termes de survie sans récidive, la survie globale ne semble guère prolongée (quelques mois) et ceci, au prix d’un coût et d’une toxicité importants. La chimiothérapie Elle concerne les mélanomes métastasés (stade IV). La dacarbazine et la fotémustine restent les drogues de référence et de première ligne. Les réponses objectivent (+ de 50 % de réduction de la masse tumorale à 3 mois) sont obtenues dans moins de 20 % des cas. Les polychimiothérapies ou les chimio-immunothérapies n’ont pas montré d’efficacité supérieure. L’évaluation du ganglion sentinelle n’a jusque-là qu’un intérêt pronostique. Surveillance Les 5 premières années constituent une période critique, puisque 90 % des récidives métastatiques ont lieu pendant cette période. Cependant, les métastases tardives sont aussi possibles. Enfin, les patients ayant eu un mélanome présentent un risque plus élevé d’un second mélanome. Pour les mélanomes de stade I et II, les recommandations européennes préconisent un dépistage des récidives loco-régionales à l’aide d’un examen clinique trimestriel les 5 premières années, puis semestriel pendant encore 5 ans. Pour les mélanomes inférieurs à 1 mm, une surveillance clinique semestrielle semble suffisante. L’examen clinique doit rechercher l’existence de nouvelles lésions pigmentées atypiques, des localisations souscutanées ou ganglionnaires superficielles. Une échographie, en particulier ganglionnaire, peut être utile pour confirmer l’examen clinique. La surveillance par scanner ou par Pet-scan n’est pas standardisée et ne fait pas l’objet de consensus. 90 % des récidives métastatiques ont lieu pendant les 5 premières années. Conclusion L’établissement de ces recommandations a permis la rencontre multidisciplinaire au niveau européen de dermatologues, d’oncologues, de chirurgiens oncologues, de radiothérapeutes et d’histopathologistes. Elles mettent cependant en évidence la triste réalité médicale du mélanome. En effet, le diagnostic repose encore uniquement sur l’examen clinique et histologique, sans aucun critère pronostique véritablement fiable actuellement bien que plusieurs marqueurs génétiques soient en cours d’évaluation. Son traitement repose toujours sur la chirurgie d’exérèse initiale et aucun traitement adjuvant ou curatif n’a montré de réels bénéfices en termes de survie globale. Enfin, la surveillance et le dépistage des récidives restent toujours aléatoires et non satisfaisants. Il reste à espérer que toutes ces insuffisances seront prochainement comblées par les progrès dans la connaissance génétique et moléculaire de la mélanocarcinogenèse.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :