Publié le 01 sep 2011Lecture 10 min
Efficacité et tolérance des biothérapies dans le psoriasis sévère
P. BERBIS Service de dermatologie, Hôpital Nord, Marseille
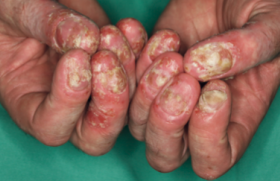
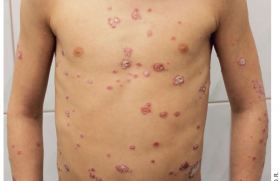
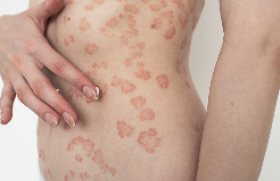
Le psoriasis est une des dermatoses les plus fréquentes puisqu’elle touche environ 3 % de la population. Les formes les plus étendues ou touchant des topographies à fort retentissement social ou fonctionnel ont un impact significatif sur la qualité de vie. Le TNFα joue un rôle déterminant dans la pathogénie des lésions ; cette découverte a conduit au développement puis à la mise sur le marché de biothérapies s’opposant à son action (traitements anti-TNF). De nouvelles voies immunopathogènes et de nouvelles molécules sont venues enrichir récemment les traitements par biothérapie. L’efficacité spectaculaire des biothérapies ne doit cependant pas faire oublier les risques, notamment infectieux et à plus long terme néoplasiques, qui doivent rester constamment à l’esprit, tant en termes de screening préthérapeutique que de dépistage au cours du traitement.
Biothérapies : efficacité L’indication des biothérapies est réservée au traitement des psoriasis en plaques sévères résistants ou présentant une contre-indication ou une intolérance à au moins deux des traitements systémiques suivants : photothérapie, méthotrexate, ciclosporine. Les anti-TNFα sont au nombre de trois (infliximab [Remicade ®], étanercept [Enbrel®], adalimumab [Humira®]). L’infliximab (INF), administré en perfusion par voie intraveineuse à la dose de 5 mg/kg à S0-S2-S6 puis toutes les 8 semaines, permet l’obtention d’un PASI75 dans 88 % des cas à S10(1), mais la poursuite du traitement dans l’étude de Reich(2) s’accompagne d’une relative perte d’efficacité avec le temps (61 % de PASI75 à 50 semaines), probablement en raison de la synthèse d’anticorps antiinfliximab. Avec l’infliximab, un ACR20 est obtenu dans 58 % des cas à S14 en cas de rhumatisme psoriasique (RP). L’étanercept (ETA), administré par voie sous-cutanée à raison de 2 injections de 50 mg par semaine, pendant 12 semaines, puis 25 mg par injection, permet l’obtention d’un PASI75 dans 56 % des cas à la 12e semaine (S12) dans l’étude de Gottlieb(3) et dans 44 % des cas à S24 dans l’étude de Leonardi(4). Dans l’étude de Mease (RP)(5), un ACR20 (critère de l’American College of Rhumatology : amélioration d’au moins 20 % des articulations douloureuses) est obtenu à S12 dans 59 % des cas (25 mg 2 fois/sem). L’adalimumab (ADA) par voie sous-cutanée à la dose initiale de 80 mg, puis 40 mg toutes les 2 semaines, entraîne dans l’étude de Menter(6) un PASI75 (amélioration d’au moins 75 % du PASI de départ) dans 71 % des cas après 16 semaines de traitement. Dans l’étude de Mease (7), des patients avec rhumatisme psoriasique (RP) reçoivent ADA 40 mg toutes les 2 semaines : à la 12e semaine, 58 % des patients atteignent un ACR20. La réponse est rapide. L’ustékinumab (Stelara®) est un anticorps monoclonal qui se lie avec la sous-unité p40 de l’IL- 12 et de l’IL-23, interrompant donc leur voie de signalisation, impliquée dans la pathogénie du psoriasis. L’étude PHOENIX 1 (8) a comparé ustékinumab 45 mg et 90 mg sous-cutané (S0, S4 puis toutes les 12 semaines) versus placebo dans le psoriasis sévère. À S12, le PASI75 est atteint chez 67 % des patients traités par ustékinumab, versus 3 % sous placebo. Le golimumab est une nouvelle molécule anti-TNF qui a été étudiée dans le RP(9). À la posologie de 50 mg en sous-cutané toutes les 4 semaines, un ACR20 est obtenu dans 51 % des cas à S24. Biothérapies : tolérance et risques potentiels Risque infectieux Il est particulièrement à redouter concernant les infections sévères, nécessitant une hospitalisation (cutanées, respiratoires, ostéoarticulaires, urinaires, etc.). Une métaanalyse des essais au cours de la polyarthrite rhumatoïde (PR) avec ADA et INF (3 493 patients traités) montre un risque accru d’infections sévères avec un odds ratio (OR) égal à 2(10). Le risque est particulièrement net en cas de fortes doses. Une autre étude au cours de la PR, ayant colligé 18 essais incluant 8 808 patients traités par biothérapies, ne montre pas de sur-risque pour des posologies recommandées (11). Le risque de tuberculose (TUB) est particulièrement à prendre en compte. Une étude de la British Society for Rheumatology (12) a conclu à une incidence de tuberculose variable selon les molécules, respectivement de 0,5, 0,9 et 1,5/1 000 patients/an respectivement pour ETA, ADA et INF. Le délai moyen de survenue est de 8 à 12 semaines pour l’INF, plus long pour les 2 autres anti- TNF (ADA et ETA). La présentation est souvent atypique, extrapulmonaire ou disséminée. Il est donc impératif de dépister toute tuberculose latente avant de débuter un traitement par biothérapie et de traiter au préalable pendant 3 mois en cas de tuberculose latente. Les éléments du dépistage reposent sur l’interrogatoire, l’examen et la réalisation d’une IDR à 5 unités de tuberculine. En 2006, la HAS a proposé l’utilisation de tests sanguins (Quantiferon®, T-SPOT®). Le diagnostic de tuberculose au cours du traitement impose un arrêt impératif immédiat de la biothérapie et un traitement complet urgent. Les infections virales sont un point important de la surveillance et du dépistage (13). • Le TNFα intervient de manière active dans le contrôle immunologique de la réplication du virus de l’hépatite B (VHB). L’utilisation des anti-TNFα chez des patients présentant une hépatite B a pu entraîner des hépatites fatales. Il convient donc de s’assurer de l’absence d’hépatite B avant d’initier le traitement. Des réactivations virales en cas d’hépatite B « guérie » (antigène HBS négatif) ont été rapportés. Dans ces cas, l’indication, si elle est impérative, doit se discuter avec l’hépatologue. • Le TNFα a une action pathogène sur l’évolution de l’hépatite C (stimulation de l’apoptose hépatocytaire et de l’inflammation hépatique). Pour les hépatologues, une plus grande tolérance peut être adoptée concernant le risque évolutif d’hépatite C sous anti-TNFα. Concernant le psoriasis, l’évaluation précise du ratio risque-bénéfice s’impose et toute décision doit être en étroite concertation avec l’hépatologue. • Si les études publiées ne montrent pas d’impact significatif des anti-TNFα sur la charge virale HIV ou le compte des lymphocytes CD4+(in 13), il faut cependant garder à l’esprit le risque d’aggraver un immunodéficit et d’exposer le patient à des infections plus sévères. • La réactivation d’infections herpétiques sous anti-TNFα paraît peu fréquente, mais suffisamment sévère, avec risque d’infection disséminée, pour faire évoquer le diagnostic systématiquement (formes atypiques) et faire stopper le traitement anti-TNF au moindre doute sur la survenue d’un herpès parallèlement à l’instauration d’un traitement. • Le risque de réactivation du virus varicelle-zona est également connu, particulièrement pour les anticorps monoclonaux (infliximab, adalimumab), avec possibilité de formes sévères ou récidivantes. Des cas de varicelles sévères (dont une fatale) ont été observés(in 13). • Des observations d’infection ou de réactivation de CMV ont été rapportées chez des patients traités par infliximab, avec hépatite, rétinite et syndrome d’activation macrophagique. Cette complication est cependant très rare (études prospectives de patients traités par infliximab pour des entéropathies inflammatoires ou polyarthrite rhumatoïde(in 13)). • Des condylomatoses ano-génitales florides ont été rapportées sous anti-TNFα imposant le dépistage systématique des infections à HPV avant traitement et une surveillance sous traitement. Pathologies démyélinisantes (revue in 14) Les biothérapies sont susceptibles d’induire ou d’aggraver des pathologies démyélinisantes ou une sclérose en plaques. Le nombre de cas est aujourd’hui très faible, et l’incidence mal connue. En cas de survenue, le délai moyen est de 5 mois. Il faudra être particulièrement attentif à des paresthésies, des troubles visuels (névrite optique), un état confusionnel. Au moindre doute, l’avis d’un neurologue s’impose. Dans la majorité des cas, une régression plus ou moins complète des symptômes a été observée à l’arrêt de la molécule. Rappelons le retrait en 2009 de l’éfalizumab (Raptiva®), biothérapie anti-CD11 en raison de l’enregistrement de cas de leucoencéphalopathie multifocale. Tout antécédent de pathologie démyélinisante est une contreindication formelle à un traitement par biothérapie. Risque néoplasique Comme avec tout traitement immunosuppresseur, le risque néoplasique est important à analyser et à prendre en compte dans la tolérance au long cours. Lymphomes Les données disponibles sont issues principalement de séries de patients traités pour polyarthrite rhumatoïde (PR), sachant qu’au cours de cette pathologie, le risque de lymphome est accru par rapport à la population générale, ce qui n’est pas le cas pour le psoriasis. Plusieurs cas de lymphomes sous biothérapies sont rapportés dans la littérature. Au terme d’une analyse des essais de développement des biothérapies dans la PR, la FDA a en 2003 évalué le SIR (Standard Incidence Ratio : rapport entre le nombre d’événements observés et le nombre d’événements attendus dans la population normale) pour les lymphomes à 5,52 pour l’ADA, 2,31 pour l’ETA et 6,35 pour l’INF (15). Les données récentes d’une très large cohorte de 19 591 patients atteints de PR traités par biothérapie indiquent un SIR de 1,8(16). Dans le psoriasis, les études prospectives sur le long terme manquent encore aujourd’hui. L’étude de Tyring (17) n’a pas montré une augmentation de l’incidence des néoplasies par rapport aux données de la population générale après 96 semaines de traitement par étanercept 25 mg 2 fois/ semaine. Un antécédent de lymphome est une contre-indication formelle à un traitement par biothérapie. Sous traitement, il faudra être particulièrement attentif à des symptômes tels qu’un amaigrissement, une asthénie persistante, des sueurs nocturnes, un prurit diffus. De même, toute lésion cutanée atypique devra être biopsiée. Cancers solides Le risque est ici encore mal évalué, et principalement dans la prise en charge de la PR. Un suivi de cohorte de 13 001 patients atteints de PR entre 1998 et 2005 a été rapporté(16) ; 49 % des cas étaient traités par biothérapie. Dans ce groupe, les auteurs n’ont pas noté de sur-risque de cancers solides extracutanés ni de sur-risque de lymphomes. En revanche, ils concluent à un risque accru de cancers cutanés non mélanocytaires (OR = 1,5) et un risque légèrement accru de mélanomes. En attendant les données relatives au traitement au long cours du psoriasis par biothérapies, il faudra être particulièrement attentif chez des patients ayant reçu d’autres immunosuppresseurs, ayant eu de nombreuses séances de photothérapie et ayant des facteurs de risque. Ces patients devront bénéficier d’un suivi et de mesures de dépistage réguliers. Perspectives : place des biothérapies dans l’amélioration des comorbidités L’association psoriasis-syndrome dysmétabolique est aujourd’hui bien admise, avec son cortège de complications cardiovasculaires. La question de l’intérêt d’un traitement précoce par biothérapie permettant de limiter ce risque cardiovasculaire est posée. La revue générale de Vena et coll. (18) fait parfaitement le point sur cette problématique de première importance. L’introduction des biothérapies permettrait-elle de réduire l’incidence et la gravité des comorbidités cardiovasculaires au cours du psoriasis ? Ce sur-risque d’événements cardiovasculaires au cours du psoriasis aujourd’hui bien démontré, pourrait être lié à une association au syndrome dysmétabolique, mais aussi au rôle de l’inflammation chronique sur les parois artérielles, à l’instar de ce que l’on observe au cours du lupus ou de la PR. Il est bien sûr trop tôt pour conclure, mais les premiers éléments issus des travaux récents semblent encourageants. Les anti-TNF améliorent la résistance à l’insuline, augmentent les taux d’adiponectine, diminuent l’épaisseur de l’intima des vaisseaux, précédée par une réduction des marqueurs de l’inflammation (vitesse de sédimentation, CRP, IL-6, fibrinogène) et améliorent la fonction endothéliale( in 18). Cependant, des prises de poids ont été observées sous anti-TNF. De nombreux travaux complémentaires restent à faire pour confirmer ces données préliminaires, mais il est possible de concevoir que l’introduction précoce d’une biothérapie dans la prise en charge d’un psoriasis sévère, surtout s’il est associé à une composante inflammatoire articulaire, pourrait limiter le risque d’altérations vasculaires.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :