Publié le 03 mar 2011Lecture 11 min
L’acné : une manifestation d’hyperandrogénisme. Comment la traiter ?
C. JAMIN, Paris

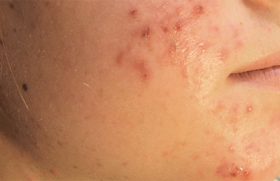
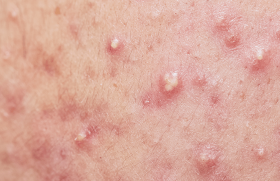
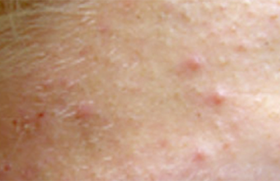
L’acné est une dermatose multifactorielle dont l’hormonodépendance est indiscutable et qui implique une hyperproduction de sébum, une kératinisation du canal excréteur des glandes sébacées et une inflammation liée à la prolifération de Propionibacterium acnes. Son apparition coïncidant avec le démarrage du fonctionnement gonadique en est une première preuve. Ainsi, la quasi-totalité des adolescents vont présenter une acné, qui s’améliore avec le temps chez la plupart, mais qui peut persister à l’âge adulte. L’efficacité des traitements hormonaux en est une autre preuve.
Le fonctionnement de la glande sébacée dépend des sécrétions gonadiques et l’amélioration des lésions acnéiques avec le temps peut être rapportée à un processus de désensibilisation des récepteurs hormonaux, assez classique en hormonologie : la réaction à un stimulus hormonal est d’autant plus importante que la glande a été sevrée de contact avec les hormones, puis elle décroît. Ainsi, la production de sébum sous l’influence des androgènes est très importante au début de l’imprégnation hormonale, puis elle diminue du fait que la glande se désensibilise. Ce phénomène de désensibilisation est bien connu avec les estrogènes : alors qu’une femme, pendant sa vie ovarienne, tolère bien des doses d’estrogènes assez importantes avec la contraception, une femme ménopausée supporte d’autant plus mal les estrogènes qu’elle est ménopausée de longue date ; l’apparition de mastodynies traduit alors une hypersensibilité aux estrogènes. Au niveau de la glande sébacée, la perte de sensibilité aux androgènes avec l’âge reste un phénomène non expliqué. Quel est l’androgène responsable de la sécrétion sébacée ? L’acné nécessite la conjonction de trois composantes : la production de sébum, la rétention, qui favorise la prolifération de P. acnes, et l’inflammation induite par cette dernière. La production de sébum est régulée par les androgènes via des récepteurs localisés dans la glande sébacée. À la puberté, marquée par la sécrétion des androgènes surrénaliens (DHEA et sulfate de DHEA), puis par celle des androgènes plus puissants, Δ4-androstènedione, testostérone, dihydrotestostérone, la glande sébacée commence à être stimulée. La seule corrélation mise en évidence à la puberté entre l’acné et les androgènes l’a été avec le DHEA-S qui circule à des taux très élevés, sans commune mesure avec celui des autres androgènes. La glande sébacée dispose de tout l’équipement enzymatique nécessaire à la transformation des androgènes (DHEA-S vers la DHEA puis vers la testostérone), si bien que même un androgène faible tel que le DHEA-S peut stimuler la glande. Elle possède notamment une 5α-réductase de type 1 qui transforme la testostérone en dihydrotestostérone (DHT), laquelle a une affinité encore plus importante pour le récepteur des androgènes (RA). L’activité transcriptionnelle de RA, dont dépend le niveau d’expression de l’androgénisation, est régulée par un corépresseur, lui-même fonction du nombre de triplets CAG présents sur l’exon 1 du gène du récepteur : plus le nombre de triplets est élevé, moins l’hormone aura d’effet sur son récepteur, et inversement. Le polymorphisme génétique de RA module ainsi les manifestations d’androgénisme, qu’il s’agisse de l’acné, de l’hirsutisme ou de l’alopécie androgénogénétique. Une question demeure encore non élucidée qui est de savoir si la testostérone est capable de stimuler directement la glande sébacée, comme dans quelques tissus (muscle) ayant une sensibilité particulière aux androgènes, y compris à des androgènes faibles comme la testostérone, sans devoir être transformée en DHT par la 5α-réductase , comme dans la plupart des tissus cibles qui ont une sensibilité plus faible. L’absence d’efficacité du blocage spécifique de la 5α-réductase de type 1 sur l’acné tendrait à prouver que la testostérone agit directement sur la glande sans transformation préalable. Autres intervenants dans la production sébacée Les estrogènes exercent un effet inhibiteur de la production de sébum par plusieurs mécanismes : ils augmentent la protéine porteuse de la testostérone (TEBG) et, par là, diminuent les taux d’hormones libres et bloquent son expression ; à dose pharmacologique, ils ont un effet inhibiteur de la 5α-réductase et de la production de sébum. Bien d’autres intervenants sont impliqués dans la production sébacée : facteurs de croissance (IGF), hormone de croissance, récepteur LXR (qui régule les gènes impliqués dans l’efflux de cholestérol et phospholipides), récepteurs PPAR (impliqués dans la croissance, la différenciation épidermique et le métabolisme des lipides), entre autres. Quelle est la place du traitement hormonal dans l’acné ? • Le traitement hormonal de lʼacné a pour objectif de soustraire les glandes sébacées à la stimulation exercée par les androgènes, donc de diminuer l’expression de la maladie. Ce traitement a un effet suspensif, contrairement à l’acide rétinoïque qui est probablement le seul traitement susceptible d’exercer un effet définitif, sans doute en favorisant l’apoptose des cellules sébacées. Le traitement hormonal permet par conséquent d’attendre que la désensibilisation des récepteurs intervienne naturellement. Quel qu’il soit, si la désensibilisation n’est pas intervenue sous traitement, l’acné réapparaîtra à son arrêt et au niveau qu’elle aurait eu en l’absence de traitement. Cela pourrait d’ailleurs expliquer l’apparition des acnés tardives ou persistantes, bien que les mécanismes de la désensibilisation des récepteurs soient imparfaitement connus. • Le premier traitement hormonal est la contraception orale estroprogestative. Le progestatif diminue la production d’androgènes d’origine ovarienne grâce à son effet antigonadotrope ; l’estrogène augmente les taux de TEBG, empêchant la libération de testostérone libre, d’où une diminution de la production sébacée androgénodépendante, et exerce un effet direct sur la production sébacée et sur la 5α-réductase à dose pharmacologique. La pilule régularise les taux de sécrétion des androgènes, en particulier chez les femmes ayant des troubles des règles et plus encore en cas de SOPK. Elle est donc active sur l’hyperandrogénisme et l’hyperandrogénie. Les pilules à l’épreuve des essais cliniques dans l’acné Certaines pilules de 1re génération contenaient des progestatifs antigonadotropes dotés d’une activité androgénique forte, ce qui amputait le bénéfice induit par l’estrogène, d’où leur responsabilité dans l’augmentation des manifestations acnéiques. Aujourd’hui, non seulement les progestatifs sont nettement moins androgéniques, mais bien davantage antigonadotropes, et ainsi utilisés à plus faible dose. Le bénéfice des pilules a été évalué dans le cadre d’une revue Cochrane (Arowojolu AO et al. 2009). Sur 7 études versus placebo, 2 ont évalué la combinaison lévonorgestrel (LNG) 100 μg/EE 20 μg, et démontré son efficacité sur l’ensemble des paramètres (nombre total de lésions, de lésions inflammatoires et non inflammatoires). Ce résultat satisfaisant a donc été obtenu avec une pilule de 2e génération au LNG à faible dose, les 20 μg d’EE étant suffisants pour obtenir un effet antiandrogène. De bons résultats ont également été obtenus dans 2 études avec des pilules triphasiques au norgestimate, de même que dans 2 études évaluant la combinaison drospirénone/EE. Dix-sept études randomisées ont comparé chacune deux pilules entre elles. Il n’a pas été mis en évidence de différence d’efficacité sur l’acné entre les différentes pilules de 3e génération ou de 3e et 4e générations ; en effet, dans une pilule comportant un progestatif non androgénique, c’est l’EE qui est le principal composant antiandrogène. En revanche, une pilule de 3e génération est légèrement plus efficace sur l’acné qu’une pilule de 2e génération à 30 μg d’EE car, dans ces dernières, la dose de LNG à 150 μg est suffisamment importante pour freiner l’effet antiandrogène de l’EE. A contrario, en diminuant la dose de LNG à 100 μg dans une pilule de 2e génération associée à 20 μg d’EE, on récupère l’effet antiandrogène de l’EE, qui se manifeste par une meilleure efficacité contre l’acné. Enfin, la comparaison des pilules de 2e et 3e générations à 20 μg d’EE montre une très légère supériorité de la 3e génération (un seul des critères étudiés était significativement différent et à un seul des temps d’évaluation). Pour obtenir un effet antiacnéique supérieur à celui des contraceptifs estroprogestatifs, il faut recourir à un progestatif antiandrogénique à dose plus élevée (au moins 25 mg acétate de cyprotérone). En pratique, quelle pilule choisir ? La prise en charge hormonale d’une femme acnéique ne doit pas être centrée uniquement sur l’acné et doit se concevoir en prenant en compte l’ensemble des risques et bénéfices escomptés de la contraception. Aujourd’hui, les autorités de santé recommandent chez les femmes tout-venant une contraception de 2e génération avec une pilule à 20 μg d’EE associée au LNG, en raison de sa meilleure sécurité en termes de risque thromboembolique veineux. Par conséquent, chez une femme ayant une acné modérée, il est préférable de prescrire ce type de pilule en première intention. Si les résultats sont insuffisants sur l’acné, on peut essayer une pilule de 3e génération à 20 μg d’EE ayant démontré son efficacité. Cependant, si l’on veut vraiment améliorer l’efficacité sur l’acné, il faudra prescrire une pilule à 30 μg d’EE associée à un progestatif de 3e génération (et non de 2e génération), et prise en charge par la Sécurité sociale, si l’on veut s’assurer de l’observance du traitement. Dans ce cadre, il n’y a aucune indication à prescrire une pilule à 30 μg ou 20 μg d’EE non remboursée. Si l’acné persiste sous contraception orale estroprogestative, après échec de deux cures d’acide rétinoïque prescrit à bonne dose et en concertation avec le dermatologue, il est licite de débuter un traitement par acétate de cyprotérone à la dose minimale de 25 mg, qui a un effet contraceptif, et en association avec 25 μg d’EE pour son effet antiacnéique ou avec Diane®. À l’arrêt de la pilule, l’acné peut réapparaître ; ce que l’on pense être une acné tardive survenant à l’arrêt de la pilule n’est en fait qu’une acné masquée. De même, l’acné peut réapparaître à l’arrêt de l’acétate de cyprotérone. Acné et contraception progestative Les contraceptions progestatives pures peuvent favoriser ou révéler une acné. Cela n’est généralement pas dû à un effet androgénique du progestatif, mais lié à la diminution de la TEBG par le progestatif, d’où une augmentation du taux de testostérone libre. Le passage d’une contraception estroprogestative à une contraception progestative ferait perdre le bénéfice de l’effet antiandrogénique de cette combinaison. Peut s’adjoindre à ces mécanismes un effet androgénique, même modeste, propre au progestatif. Une exploration hormonale est rarement nécessaire chez la femme acnéique L’objectif d’une exploration hormonale est ici de différencier hyperandrogénie et hyperandrogénisme. Comme il n’y a pas d’hyperandrogénie en l’absence de trouble des règles, il est inutile de faire un bilan hormonal chez une femme acnéique ayant des règles régulières de 28 ± 2 jours. Le bilan (estradiol, testostérone, FSH, LH, AMH, prolactine) est justifié en présence de règles irrégulières, persistant 2 ans après la puberté. La prise en charge des manifestations cutanées du SOPK ne diffère pas beaucoup de celle de l’hyperandrogénisme : les estroprogestatifs sont efficaces en bloquant la fonction ovarienne et la production de testostérone ; la perte de poids diminue la sécrétion d’androgènes ; la metformine, en diminuant l’insulinorésistance, a un effet modeste sur les androgènes sécrétés par l’ovaire polykystique. Il existe d’autres causes d’hyperandrogénie, rares et toujours associées à des troubles des règles. Seul le bloc surrénalien congénital à révélation tardive, qui dans sa forme hétérozygote peut s’accompagner de règles normales, peut poser problème. En pratique, le bilan hormonal doit être réalisé après au moins 2 mois d’arrêt de la pilule, au 2e ou 3e jour des règles ; en effet, une élévation de la Δ4- androstènedione, de la 17-OHprogestérone ou de la testostérone en deuxième partie de cycle est ininterprétable.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :