Publié le 11 déc 2016Lecture 6 min
Maladie d’Erdheim-Chester : une histiocytose grave - Intérêt des signes dermatologiques pour un diagnostic précoce
P. BERBIS, Hôpital Nord, CHU de Marseille
Un homme de 24 ans, en bon état général, consultait pour le développement de lésions initialement papuleuses, puis rapidement nodulaires au niveau du tronc, non prurigineuses…
Observation
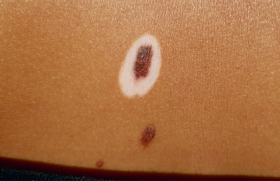
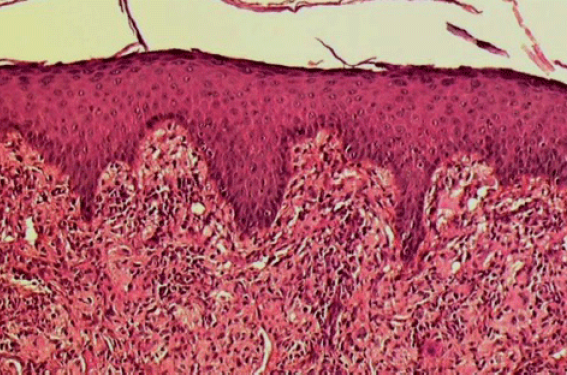
Un homme de 24 ans, en bon état général, consultait pour le développement de lésions initialement papuleuses, puis rapidement nodulaires au niveau du tronc, non prurigineuses (figure 1). Le reste de l’interrogatoire et de l’examen clinique était sans anomalie, il décrivait tout au plus de vagues douleurs osseuses des membres inférieurs et une asthénie peu intense d’apparition récente. Il ne prenait aucun traitement et n’avait pas d’antécédents particuliers. Un diagnostic de sarcoïdose avait été porté récemment et un traitement par hydroxychloroquine s’était révélé sans efficacité et avait été stoppé. La biopsie d’un nodule montrait une infiltration dermique superficielle et profonde faite de cellules histiocytaires de Touton, spumeuses, l’ensemble donnant un aspect de xanthogranulome (figures 2 et 3).
Figure 1. Lésions nodulaires du tronc.
Figure 2. Infiltrat dermique xanthogranulomateux.
Figure 3. Cellules de Touton.
Des cellules géantes plurinucléées étaient notées. Les immunomarquages montraient un marquage très positif pour le CD68 (figure 4), plus faible pour la protéine S100, mais totalement négatif pour le CD1a (figure 5). Le diagnostic d’histiocytose non langheransienne était retenu. Le bilan biologique était normal, notamment au plan hématologique, hépatique, rénal, immunologique et infectieux.
Figure 4. Marquage positif au CD68.
Figure 5. Marquage négatif au CD1a.
La scintigraphie osseuse au 99 Te montrait des hyperfixations nettes au niveau des régions métaphyso-diaphysaires des os longs (figure 6). L’examen ophtalmologique montrait une discrète inflammation de la chambre antérieure des deux yeux. Les radiographies du crâne, du thorax et l’échographie abdomino-pelvienne étaient normales. Le scanner TAP montrait un épaississement périaortique de l’ensemble des segments s’étendant à l’aorte sus-, inter- et sous-rénale et à l’artère iliaque gauche réalisant l’aspect de coated aorta (figure 7).
Figure 6. Scintigraphie osseuse : hyperfixations métaphyso-diaphysaires intenses.
Figure 7. Coated aorta.
L’échocardiographie montrait une tumeur adhérente à la paroi septale de l’oreillette gauche. Le diagnostic d’histiocytose non langheransienne à type de maladie d’Erdheim-Chester a été retenu et un traitement par cladribine débuté.
Discussion
La maladie d’Erdheim-Chester (MEC) est une histiocytose non langheransienne (HNL) d’étiologie inconnue. Elle a été décrite en 1930. Depuis, moins de 1 000 cas seulement ont été rapportés. Il s’agit très certainement d’une pathologie sousdiagnostiquée. Le sex ratio est de 7 hommes pour 3 femmes. L’âge moyen est de 50 ans au moment du diagnostic, mais des observations touchant les adultes jeunes, comme dans notre observation, ou des formes gériatriques ont été rapportées. La MEC est de mauvais pronostic avec une médiane de survie de 20 mois en l’absence de traitement(1). La MEC appartient au groupe hétérogène des histiocytoses non langerhansiennes non malignes, non ou inconstamment régressives, parmi lesquelles sont inclus le xanthoma disseminatum de Montgomery, la réticulo-histiocytose multicentrique, l’histiocytose nodulaire progressive, l’histiocytose mucineuse progressive héréditaire et la MEC. L’ensemble des manifestations cliniques est non spécifique, ce qui explique un diagnostic souvent tardif. L’importance des signes dermatologiques est, de ce fait, à souligner, mettant le dermatologue au premier plan d’un diagnostic souvent difficile.
Atteinte cutanéo-muqueuse
Les manifestations cutanéomuqueuses sont inconstantes mais combien importantes pour le diagnostic. Un xanthélasma est présent dans 30 % des cas, une atteinte des muqueuses génitales est beaucoup plus rare. La forme nodulaire de notre observation est exceptionnelle. L’analyse anatomopathologique fait le diagnostic en montrant un infiltrat xanthogranulomateux composé d’histiocytes et de macrophages chargés en graisse et entourés de fibrose. Les cellules histiocytaires ne sont pas des cellules de Langerhans (pas de granules de Birbeck, faible marquage à la protéine S100, marquage positif au CD68, négativité du CD1a).
Atteinte osseuse
L’atteinte osseuse est caractéristique de la MEC. Son expression radiologique est quasi constante. La symptomatologie clinique, à type de douleurs osseuses vagues, peu intenses, prédominant au niveau des membres inférieurs, n’est pas d’un grand secours diagnostique.
La scintigraphie osseuse au 99 Te est incontournable dans le bilan d’une MEC, montrant typiquement des hyperfixations au niveau des régions métaphyso-diaphysaires des os longs, principalement des membres inférieurs. Le TEP scanner est également très utile pour dépister ou confirmer ces atteintes osseuses.
Atteinte cardiovasculaire
Les manifestations cardiovasculaires font le pronostic de la MEC. L’aspect le plus caractéristique, particulièrement net dans notre observation, est l’engainement péri-aortique, qui peut toucher tous les segments de l’aorte (thoracique, abdominal). On parle de coated aorta lorsque tous les segments de l’aorte sont touchés. Cet aspect très particulier, à forte valeur diagnostique, traduit l’infiltration des tissus aortiques et péri-aortiques par des histiocytes. Le tropisme des histiocytes pour l’intima est particulièrement net, l’adventice étant, quant à elle, le siège d’une fibrose. La coated aorta est, au sein des histiocytoses, spécifique de la MEC. Dans la série d’Haroche et coll. en 2004(2), cette atteinte était notée chez 40 des 178 cas de la littérature. Cette atteinte est asymptomatique pendant longtemps. L’extension peut se faire aux branches de l’aorte. Elle peut alors, selon la localisation et l’intensité, être responsable de manifestations ischémiques (infarctus du myocarde, angor mésentérique, accident vasculaire cérébral, hypertension artérielle [atteinte vasculaire rénale pouvant être accessible à une angioplastie]). Le diagnostic différentiel peut se poser avec une artérite de Takayashu, vascularite touchant des femmes jeunes et d’expression angiographique différente.
Les atteintes cardiaques sont également décrites. L’infiltration du péricarde (42 % des cas dans la revue d’Haroche et coll.(2)) peut, dans les cas les plus graves, être responsable d’une tamponnade. Des pseudo-tumeurs atriales droites ont été observées, de même que des atteintes valvulaires aortiques et mitrales. L’échocardiographie doit donc faire partie du bilan systématique d’une MEC. De rares cas de thrombose veineuse par compression extrinsèque ont été rapportés.
Atteinte rétro-orbitaire
L’atteinte rétro-orbitaire (25 % des cas) est responsable d’une exophtalmie, moins spectaculaire que dans la maladie de Basedow cependant.
Atteinte endocrinienne
Le diabète insipide est la manifestation la plus fréquente. Beaucoup plus rarement ont été rapportés un hypogonadisme, une hyperprolactinémie. L’infiltration des surrénales est fréquente (30 % des cas), mais exceptionnellement responsable d’une insuffisance surrénalienne. Une fibrose rétropéritonéale est également rencontrée dans 30 % des cas.
Atteinte pulmonaire
Elle est beaucoup plus rare (1 cas sur 5). À la différence d’autres histiocytoses, notamment langerhansiennes, elle est rarement sévère. Le scanner thoracique doit faire partie du bilan systématique d’une MEC à la recherche d’une atteinte parenchymateuse (épaississement des septa interlobulaires, plages en verre dépoli). En l’absence de traitement, l’évolution vers l’insuffisance respiratoire est possible.
Atteinte neurologique
Rare (1 cas sur 4), elle signe une forme de mauvais pronostic. Toutes les manifestations sont possibles (comitialité, syndrome pyramidal, syndrome cérébelleux, atteinte des paires crâniennes). Le TEP scanner est très utile, notamment pour faire état de l’extension de l’infiltration histiocytaire des organes, particulièrement cardiovasculaire et osseux. Il doit faire partie du bilan initial d’une MEC.
Traitement
Le traitement de la MEC n’est pas codifié. Les corticoïdes par voie générale ont une efficacité très limitée. L’interféron alpha, surtout dans la forme pégylée, est la première molécule ayant permis d’améliorer significativement le pronostic de la MEC, à la posologie de 3 millions d’unités 3 fois par semaine(3). Les atteintes osseuses et aortiques sont celles qui répondent le mieux. L’atteinte neurologique est, en revanche, peu sensible. La nécessité d’un traitement prolongé peut poser des problèmes de tolérance au long cours. La cladribine a été proposée dans quelques observations, notamment ophtalmologiques(4). Une mutation activatrice de BRAF (proto- oncogène) a été mise en évidence dans 50 % des cas de MEC par l’équipe d’Haroche(5), offrant un rationnel très intéressant à l’utilisation du vémurafénib, inhibiteur de BRAF, qui a montré un effet très intéressant, voire spectaculaire dans quelques cas(1,6).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :